题目内容
某有机物9.2g完全燃烧,要耗氧气19.2g,生成 二氧化碳17.6g,水10.8g,试判断该有机物中
- A.只含有C、H元素
- B.只含C、H、O元素
- C.不只含C、H、O元素
- D.不含O元素
B
分析:给出具体数值的相关反应,推断物质的组成元素要根据质量守恒定律进行计算.
解答:方法1:计算氧元素的前后质量关系:
二氧化碳中氧元素的质量17.6g×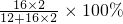 =12.8g.
=12.8g.
水中的氧元素的质量10.8g×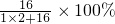 =9.6g
=9.6g
生成物含氧元素共计12.8g+9.6g=22.4g>19.2g,所以可以确定该有机物一定含有氧元素.而生成二氧化碳和水,可说明有机物中含有碳元素和氢元素.即该有机物含有碳元素、氢元素和氧元素.故选B.
方法2:计算碳元素和氢元素的质量和.
二氧化碳中碳元素的质量17.6g×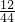 ×100%=4.8g.
×100%=4.8g.
水中的氢元素的质量10.8g× ×100%=1.2g
×100%=1.2g
生成物含氢元素和碳元素的质量和4.8g+1.2g=6g<9.2g,所以该有机物中一定含有氧元素,所以该有机物含有碳元素、氢元素和氧元素.
故选:B.
点评:给出质量关系的就要根据元素质量的质量关系进行计算,从而判断给出的物质是否含有某些元素.
分析:给出具体数值的相关反应,推断物质的组成元素要根据质量守恒定律进行计算.
解答:方法1:计算氧元素的前后质量关系:
二氧化碳中氧元素的质量17.6g×
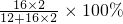 =12.8g.
=12.8g.水中的氧元素的质量10.8g×
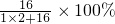 =9.6g
=9.6g生成物含氧元素共计12.8g+9.6g=22.4g>19.2g,所以可以确定该有机物一定含有氧元素.而生成二氧化碳和水,可说明有机物中含有碳元素和氢元素.即该有机物含有碳元素、氢元素和氧元素.故选B.
方法2:计算碳元素和氢元素的质量和.
二氧化碳中碳元素的质量17.6g×
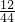 ×100%=4.8g.
×100%=4.8g.水中的氢元素的质量10.8g×
 ×100%=1.2g
×100%=1.2g生成物含氢元素和碳元素的质量和4.8g+1.2g=6g<9.2g,所以该有机物中一定含有氧元素,所以该有机物含有碳元素、氢元素和氧元素.
故选:B.
点评:给出质量关系的就要根据元素质量的质量关系进行计算,从而判断给出的物质是否含有某些元素.

练习册系列答案
相关题目