题目内容
4.下列A~E是初中化学中的五个实验装置,请按要求填空: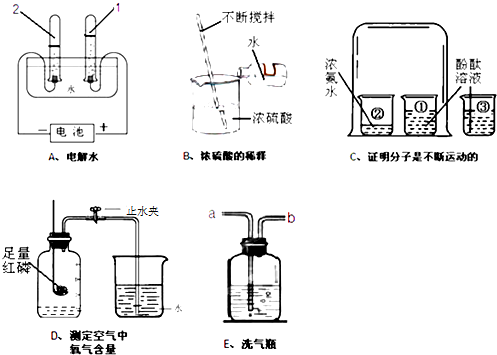
(1)A实验试管2中产生的气体是氢气(H2),试管1和2产生气体的体积比约为1:2.
(2)C实验中烧杯3的作用是作对比或对比实验;
(3)D实验说明氧气的体积约占空气的$\frac{1}{5}$,下列操作不妥的是④.
①检查装置气密性 ②实验前夹紧止水夹
③冷却后再打开止水夹 ④选用教室内的空气
(4)若用E装置除去O2中的水蒸气,该液体试剂为浓硫酸,医院还用此装置来观察给病人输氧情况,导管b(填“a”或“b”)应连接病人吸氧气的塑胶管.
(5)上述实验中操作错误的是B(填字母).
分析 根据已有的知识进行分析,电解水时生成的氢气和氧气的体积比为2:1;设计实验证明分子的运动需要设计对照试验,酚酞可使碱性溶液变红;根据测定氧气的含量实验进行分析;浓硫酸具有吸水性;稀释浓硫酸时,要将浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌.
解答 解:(1)据图可以看出2试管中产生的气体体积大,是氢气,故填:氢气;
(2)因为酚酞遇碱变红,烧杯①中的酚酞变红,说明浓氨水的化学性质是呈碱性;烧杯③是想说明酚酞在空气中不变色,起到了对比的作用,故填:呈碱性;对比;
(3)C实验是为说明氧气约占空气体积的$\frac{1}{5}$;
①红磷足量能将氧气全部消耗尽,合理;
②实验前夹紧止水夹能防止燃烧时温度升高将瓶中的其他气体排出瓶,合理;
③冷却后打开止水夹能测定的准确,合理;
④教室内由于学生多,消耗较多的氧气,故不能准确反映出空气中的氧气含量,不合理;
故填:氧气约占空气体积的 $\frac{1}{5}$;④;
(4)浓硫酸具有吸水性,能作干燥剂;从b管中出来的气体是经过浓硫酸干燥的气体,故导管b应连接病人吸氧气的塑胶管;故填:浓硫酸;b;
(5)稀释浓硫酸时,浓硫酸的密度比水的密度大,要将浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌及时散热,若将水倒入浓硫酸中容易造成液滴飞溅,图B中稀释浓硫酸将水倒入浓硫酸中操作错误,故答案:B.
故答案:(1)氢气(H2);1:2;(2)作对比或对比实验;(3)$\frac{1}{5}$;④(4)浓硫酸;b;(5)B.
点评 本题考查了水的电解的知识以及氧气含量的测定和二氧化碳的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
14.国际上以碳12原子质量的$\frac{1}{12}$作为相对原子质量的标准,碳12原子的核内有6个质子和6个中子,碳14原子在考古学中常被用来测定出土文物的年代,该原子的核内有6个质子和8个中子,下列关于碳12原子和碳14原子的说法中,不正确的是( )
| A. | 碳14原子的质量比碳12原子的质量大 | |
| B. | 碳14的原子核内质子数为6 | |
| C. | 碳14原子核内有中子数6 | |
| D. | 碳12原子和碳14原子的核外电子数为6 |
9.在密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
下列说法正确的是( )
| 物质 | X | Y | Z | W |
| 反应前的质量/g | 2 | 1 | 16 | 16 |
| 反应后的质量/g | 17 | m | 6 | 11 |
| A. | 该反应中,X、Y是反应物,Z、W是生成物 | |
| B. | 该反应的基本类型为分解反应 | |
| C. | m=1 | |
| D. | 该反应中,参加反应的Z与W的质量比为6:11 |
16.生活中常见的下列变化属于化学变化的是( )
| A. | 灯泡发光 | B. | 车胎爆裂 | C. | 蜡烛熔化 | D. | 食物腐烂 |
13.CO和CO2混合气体含碳元素36%,取此混合气体10g,通过足量灼热的CuO后,将气体通过足量的澄清石灰水,得到白色沉淀的质量是( )
| A. | 5g | B. | 10g | C. | 20g | D. | 30g |