题目内容
1.6.5g不纯的锌样品(只含一种杂质),与足量盐酸反应后,共得到0.18g氢气,此样品中含有的一种杂质可能是( )| A. | Cu | B. | Mg | C. | Al | D. | Fe |
分析 采用极值法先计算纯锌6.5g能生成氢气的质量,然后再确定杂质的类别.
解答 解:6.5g锌、镁、铝、铁与足量的盐酸反应能生成氢气的质量分别为$\frac{2}{65}$×6.5g>0.18g、$\frac{2}{24}$×6.5g>0.18g、$\frac{3}{27}$×6.5g>0.18g、$\frac{2}{56}$×5.6g>0.18g,而铜不反应,不能产生氢气,根据平均值法,若是锌与铁或镁或铝的混合物,则生成的氢气质量应该大于0.2g,不可能为0.18g,故混有的杂质是铜;
故选A.
点评 本题考查了混合金属与酸反应生成氢气的质量关系,完成此类题目,可以首先采用极值法,然后采用平均值法进行.

练习册系列答案
相关题目
11.在空气中点燃镁条时,夹持镁条应该用( )
| A. | 坩埚钳 | B. | 试管夹 | C. | 手 | D. | 止水夹 |
12.下列混合物遇到明火,不可能发生爆炸的是( )
| A. | 空气中的面粉粉尘 | B. | 空气中的煤粉粉尘 | ||
| C. | 氢气和空气 | D. | 二氧化碳和氧气 |
9.下列物质的俗名与化学式相符合的是( )
| A. | 小苏打-Na2CO3 | B. | 干冰-H2O | C. | 熟石灰-CaO | D. | 石灰石-CaCO3 |
16.除去下列物质括号中杂质的方法正确的是( )
| A. | FeO(Fe):滴加足量稀盐酸,过滤 | |
| B. | CO(CO2):将气体在空气中点燃 | |
| C. | Cu(NO3)2溶液(AgNO3):加入过量的铜粉 | |
| D. | KCl溶液(CaCl2):加入适量Na2CO3溶液,过滤 |
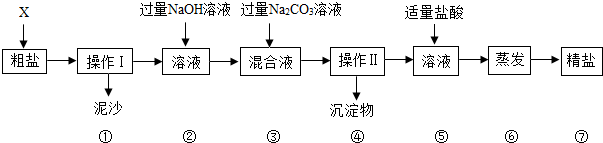
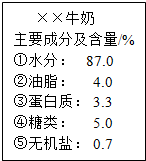 如图为某品牌牛奶的部分标签,请据此回答下列问题:
如图为某品牌牛奶的部分标签,请据此回答下列问题: