题目内容
13.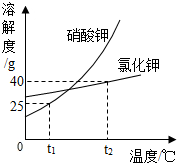 硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:
硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:(1)t1℃时,两物质中溶解度较大的是氯化钾.
(2)t2℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的饱和(填“饱和”或“不饱和”)溶液.保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数不变(填“变大”、“不变”或“变小”).
(3)硝酸钾作为化学肥料,其中的营养元素K、N.
(4)用50g蒸馏水配制t1℃时硝酸钾的饱和溶液,需硝酸钾固体的质量是12.5g,操作步骤是:计算、称量、溶解.
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钾两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钾大;t1℃时,两物质中溶解度较大的是氯化钾;t2℃时,氯化钾的溶解度是40g,因此将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的饱和溶液;保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数不变,因为烧杯底部还有剩余固体,溶液是原温度下的饱和溶液.硝酸钾作为化学肥料,其中的营养元素钾元素和氮元素;t1℃时硝酸钾的溶解度是25g,因此用50g蒸馏水配制t1℃时硝酸钾的饱和溶液,需硝酸钾固体的质量是12.5g,操作步骤是:计算、称量、溶解、装瓶存放.
解答 解:(1)t1℃时,两物质中溶解度较大的是氯化钾;故答案为:氯化钾
(2)t2℃时,氯化钾的溶解度是40g,因此将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的饱和溶液;保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数不变,因为烧杯底部还有剩余固体,溶液是原温度下的饱和溶液;故答案为:饱和;不变
(3)硝酸钾作为化学肥料,其中的营养元素钾元素和氮元素,故答案为:K、N,
(4)t1℃时硝酸钾的溶解度是25g,因此用50g蒸馏水配制t1℃时硝酸钾的饱和溶液,需硝酸钾固体的质量是12.5g,操作步骤是:计算、称量、溶解、装瓶存放;故答案为:12.5g 溶解(或量取、溶解)
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
3.下列有关物质的应用错误的是( )
| A. |  用活性炭脱色制白糖 | B. |  氧气用于航天 | ||
| C. |  用熟石灰做补钙剂 | D. |  用液氮冷冻麻醉 |
4.下列各组物质在溶液中能大量共存的是( )
| A. | CaCl2、NH4NO3、Ca(OH)2 | B. | FeCl3、Na2SO4、Mg(NO3)2 | ||
| C. | AlC13、Ba(NO3)2、Na2CO3 | D. | NH4HCO3、AgNO3、BaCl2 |
1.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 通过足量氢氧化钠溶液,并干燥 |
| B | H2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C | N2 | O2 | 通过炽热的木炭 |
| D | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
8.实验是化学学习的重要手段,通过实验可以发现和验证化学的原理,学习探究的方法并获取新知识.
Ⅰ.根据下列实验室制备气体的有关装置图回答有关问题:
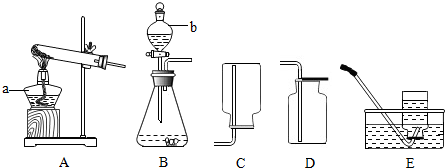
(1)写出仪器a、b的名称.a是酒精灯;b是分液漏斗.
(2)若用A装置制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择A(填编号,下同),收集较纯净甲烷应选E;请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
Ⅱ.松花蛋,又称皮蛋是餐桌一美味.加工松花蛋的一种工艺的主要原料为:鸭蛋、水、生石灰、纯碱、食盐.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【作出假设】①甲同学推断:NaOH、NaCl
②乙同学推断:NaOH、NaCl、Na2CO3
③丙同学推断:NaOH、NaCl、Ca(OH)2
④丁同学推断:NaOH、NaCl、Ca(OH)2、Na2CO3
通过进一步讨论,大家一致认为丁同学的推断是错误的,理由是(用化学方程式表示)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【实验探究】
【知识应用】皮蛋食用时加入一些食醋,可以去除涩感,原因是酸碱中和反应.
Ⅰ.根据下列实验室制备气体的有关装置图回答有关问题:

(1)写出仪器a、b的名称.a是酒精灯;b是分液漏斗.
(2)若用A装置制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择A(填编号,下同),收集较纯净甲烷应选E;请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
Ⅱ.松花蛋,又称皮蛋是餐桌一美味.加工松花蛋的一种工艺的主要原料为:鸭蛋、水、生石灰、纯碱、食盐.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【作出假设】①甲同学推断:NaOH、NaCl
②乙同学推断:NaOH、NaCl、Na2CO3
③丙同学推断:NaOH、NaCl、Ca(OH)2
④丁同学推断:NaOH、NaCl、Ca(OH)2、Na2CO3
通过进一步讨论,大家一致认为丁同学的推断是错误的,理由是(用化学方程式表示)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 | 丙同学的推断是正确的. |
| 另取少量上层料液,滴加碳酸钠溶液 | 生成白色沉淀 |
2.已知:Al(OH)3可与NaOH溶液反应,生成能溶于水的NaAlO2,即:Al(OH)3+NaOH=NaAlO2+2H2O,Mg(OH)2不与NaOH溶液反应,Mg(OH)2═MgO+H2O.现将ag镁铝合金粉末溶于足量的盐酸中,再加过量的氢氧化钠溶液,过滤,将沉淀进行洗涤、干燥、充分灼烧,得到白色粉末的质量还是ag,则原合金中镁的质量分数为( )
| A. | 60% | B. | 70% | C. | 80% | D. | 无法确定 |
3.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 向澄清石灰水中通入少量的CO2:Ca(OH)2+CO2=CaCO3↓+H2O 复分解反应 | |
| B. | 用稀硫酸洗去附着在试管壁上的铜:Cu+H2SO4=CuSO4+H2↑ 置换反应 | |
| C. | 铁丝在氧气中燃烧的反应:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 化合反应 | |
| D. | 工业制取二氧化碳:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 |