题目内容
现有一氧化碳和二氧化碳的气体混合物,若使其中的一氧化碳完全转化为二氧化碳,则得到的气体的质量比原来增加了32%.那么,原混合气体中一氧化碳和二氧化碳的分子个数比是
- A.1:2
- B.2:1
- C.2:3
- D.3:2
B
分析:得到的气体的质量比原来增加了32%,即在一氧化碳与氧气反应生成二氧化碳的反应中氧气质量为原来气体质量的32%;通过假设原来气体的质量,计算原气体中一氧化碳与二氧化碳的质量关系,使用相对分子质量求出气体中一氧化碳与二氧化碳的分子个数比.
解答:假设原混合气体质量为100,根据题意,与一氧化碳反应的氧气的质量=100×32%
设原混合气体中一氧化碳的质量为x
2CO+O2 2CO2
2CO2
56 32
x 100×32%
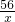 =
=
x=56
则原混合气体中一氧化碳与二氧化碳的质量比=56:(100-56)=56:44
原混合气体中一氧化碳和二氧化碳的分子个数比=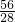 :
: =2:1
=2:1
故选B.
点评:根据反应特点,确定气体增加量为氧气的质量是解答此题的关键点,然后利用相对分子质量建立起宏观质量与微观粒子个数关的关系.
分析:得到的气体的质量比原来增加了32%,即在一氧化碳与氧气反应生成二氧化碳的反应中氧气质量为原来气体质量的32%;通过假设原来气体的质量,计算原气体中一氧化碳与二氧化碳的质量关系,使用相对分子质量求出气体中一氧化碳与二氧化碳的分子个数比.
解答:假设原混合气体质量为100,根据题意,与一氧化碳反应的氧气的质量=100×32%
设原混合气体中一氧化碳的质量为x
2CO+O2
 2CO2
2CO256 32
x 100×32%
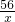 =
=
x=56
则原混合气体中一氧化碳与二氧化碳的质量比=56:(100-56)=56:44
原混合气体中一氧化碳和二氧化碳的分子个数比=
 :
: =2:1
=2:1故选B.
点评:根据反应特点,确定气体增加量为氧气的质量是解答此题的关键点,然后利用相对分子质量建立起宏观质量与微观粒子个数关的关系.

练习册系列答案
相关题目
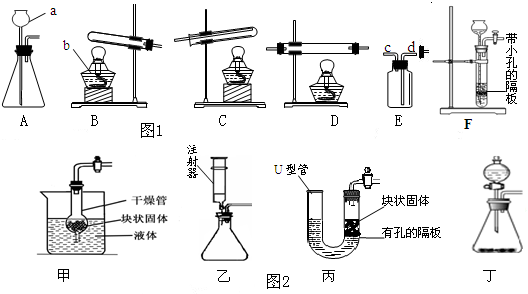
一氧化碳和二氧化碳是我们熟悉的两种重要气体,下面我们一起来完成它们的区别和检验的实验。
(1)下面实验设计有两种方法不能区别一氧化碳和二氧化碳,它们是___①___,另一个
设计在实验时能看到的明显现象是___②___。
 |
A.闻气味 B.分别通入装有水的烧杯中 C.分别通入装有紫色石蕊试液的试管中
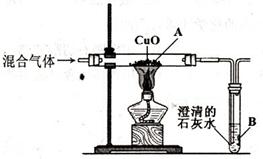
(2)现有一氧化碳和二氧化碳的混合气体,为了检验两种气体的存在,用如下装置进行实验:
实验中B装置中石灰水变浑浊,但同学们认为这个装置不能验证原混合气体中有二氧化
碳,理由是__________________①__________________。为了验证原混和气体中二氧化
碳的存在,你的改进方法是_______________________②_______________________;
写出B装置中发生反应的化学方程式__________③__________;若原混合和气体中的二氧化
有一氧化碳,则A装置中实验现象是_________________④_________________;从环保角度
看,该实验装置中的不足之处是__________________⑤__________________。