题目内容
17. 几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭号各表示一个化学反应,部分反应物、生成物及反应条件略去).已知五种物质均由C、H、O中部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和D可以发生化合反应.
几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭号各表示一个化学反应,部分反应物、生成物及反应条件略去).已知五种物质均由C、H、O中部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和D可以发生化合反应.(1)E的名称是过氧化氢,A的一种用途是冶炼金属.
(2)写出X→D转化的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(3)实现A→B转化的化学反应类型不一定(填“一定”或“不一定”)属于化合反应.
分析 根据五种物质均由C、H、O中部分元素组成,X为单质,A为有毒气体,A和B所含元素相同,因此A是一氧化碳,B是二氧化碳,所以X是氧气;D和E所含元素相同,X为氧气,B-二氧化碳和D可以发生化合反应,因此D是水,E是过氧化氢,然后将推出的物质进行验证即可.
解答 解:(1)五种物质均由C、H、O中部分元素组成,X为单质,A为有毒气体,A和B所含元素相同,因此A是一氧化碳,B是二氧化碳,所以X是氧气;D和E所含元素相同,X为氧气,B-二氧化碳和D可以发生化合反应,因此D是水,E是过氧化氢,经过验证,推导正确,所以E是过氧化氢,A是一氧化碳,可以用来冶炼金属;
(2)X→D的转化是氢气和氧气在点燃的条件下生成水,化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)A→B的转化是一氧化碳产生二氧化碳,可以是一氧化碳燃烧发生化合反应,也可以是一氧化碳还原金属氧化物产生二氧化碳,不是化合反应,因此实现A→B转化的化学反应类型不一定属于化合反应.
故答案为:(1)过氧化氢,冶炼金属;
(2)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)不一定.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
7.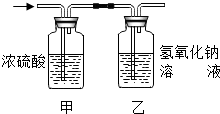 某有机物3.2g在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:分析上表的数据,该有机物的化学式是( )
某有机物3.2g在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:分析上表的数据,该有机物的化学式是( )
 某有机物3.2g在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:分析上表的数据,该有机物的化学式是( )
某有机物3.2g在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:分析上表的数据,该有机物的化学式是( )| 装置甲 | 装置乙 | |
| 通气前质量 | 200g | 180g |
| 通气后质量 | 203.6g | 184.4g |
| A. | CH4 | B. | C2H4 | C. | C2H5OH | D. | CH3OH |
8.化学家已创造出了对CO2具有较强吸收能力的粉状物质--“干水”,它每个颗粒中含水95%,外层是SiO2.下列说法中正确的是( )
| A. | 干水是一种混合物 | |
| B. | 干水吸收CO2的过程中只发生物理变化 | |
| C. | 干水和干冰都是氧化物 | |
| D. | 干水中的水分子和普通的水分子化学性质不同 |
5.学习科学知识有时需要联想和类比,卢瑟福研究发现的原子结构模型称为太阳系模型,如果把太阳系中绕太阳公转的八大行星看做原子中的八个核外电子的话,那么( )
| A. | “太阳”相当于一个原子 | B. | “太阳”中肯定有八个质子 | ||
| C. | “太阳”中肯定有八个中子 | D. | 太阳系相当于一个碳原子 |
2.化学变化中,同种元素可以在不同物质中“旅行”,下列转化关系中不符合“甲?乙?丙”“旅行”路线的是( )
| 甲 | 乙 | 丙 | 旅行元素 | |
| A | Cu | Cu(NO3)2 | Cu(OH)2 | Cu |
| B | O2 | CO2 | H2CO3 | O |
| C | H2 | H2O | Ca(OH)2 | H |
| D | CaO | Ca(OH)2 | CaCO3 | Ca |
| A. | A | B. | B | C. | C | D. | D |
9.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解化学方程式如下:
①2KNO3 $\frac{\underline{\;加热\;}}{\;}$2KNO2+O2↑;
②2Cu(NO3)2$\frac{\underline{\;加热\;}}{\;}$2CuO+4NO2↑+O2↑;
③2AgNO3$\frac{\underline{\;加热\;}}{\;}$2Ag+2NO2↑+O2↑;
又知NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3
某固体可能由上述三种硝酸盐中的一种或几种组成.取适量该固体充分加热,得到一定量的气体,将这些气体通入适量的水中,结果全部被吸收,没有剩余,则该固体组成是( )
①2KNO3 $\frac{\underline{\;加热\;}}{\;}$2KNO2+O2↑;
②2Cu(NO3)2$\frac{\underline{\;加热\;}}{\;}$2CuO+4NO2↑+O2↑;
③2AgNO3$\frac{\underline{\;加热\;}}{\;}$2Ag+2NO2↑+O2↑;
又知NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3
某固体可能由上述三种硝酸盐中的一种或几种组成.取适量该固体充分加热,得到一定量的气体,将这些气体通入适量的水中,结果全部被吸收,没有剩余,则该固体组成是( )
| A. | KNO3、Cu(NO3)2 | B. | KNO3 | ||
| C. | Cu(NO3)2 | D. | KNO3、Cu(NO3)2、AgNO3 |
6.常见金属R与硝酸银溶液反应的化学方程式为R+3AgNO3═3Ag+R(NO3)3,有关该反应的说法正确的是( )
| A. | 该反应属于置换反应 | B. | 该金属可能是锌 | ||
| C. | R的活泼性比Ag弱 | D. | R(NO3)3不溶于水 |
7.某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示.
请分析上表,并回答下列问题:
(1)该花汁可以(填“可以”或“不可以”)作酸碱指示剂.
(2)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)常用于治疗胃酸过多症,写出氢氧化铝治疗胃酸过多症时的化学反应方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)石灰水暴露于空气中易变质,写出石灰水变质的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
(1)该花汁可以(填“可以”或“不可以”)作酸碱指示剂.
(2)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)常用于治疗胃酸过多症,写出氢氧化铝治疗胃酸过多症时的化学反应方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)石灰水暴露于空气中易变质,写出石灰水变质的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
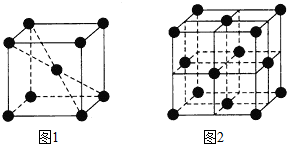 910℃以下纯铁晶体的基本结构单元如图1所示,910℃以上转变为图2所示的结构单元,在两种晶体中最邻近的铁原子间距离相同.
910℃以下纯铁晶体的基本结构单元如图1所示,910℃以上转变为图2所示的结构单元,在两种晶体中最邻近的铁原子间距离相同.