题目内容
有一铜粉和氧化铜的混合物,取混合物9g在空气中进行充分加热,待粉末颜色无变化后冷却、称量,其质量为10g,则原混合物中铜元素的质量分数为( )
| A、44.4% | B、75% |
| C、88.9% | D、94.2% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:最后得到的10g为氧化铜的质量,原混合物中铜元素即为10g氧化铜中铜元素的质量,根据10g氧化铜的质量求得原混合物中铜元素的质量,然后得出质量分数.
解答:解:最后得到的10g为氧化铜的质量,原混合物中铜元素即为10g氧化铜中铜元素的质量.
原混合物中铜元素的质量:10g×
×100%=8g
则原混合物中铜元素的质量分数为:
×100%=88.9%
故选C.
原混合物中铜元素的质量:10g×
| 64 |
| 64+16 |
则原混合物中铜元素的质量分数为:
| 8g |
| 9g |
故选C.
点评:本题主要考查学生分析数据,找出规律的能力.

练习册系列答案
相关题目
下列有关二氧化碳的性质、验满、制备和用途能达到目的是( )
| A、用二氧化碳做气体肥料 |
| B、二氧化碳气体通入紫色石蕊试液中,溶液变为蓝色 |
| C、用块状石灰石和稀硫酸迅速制备大量二氧化碳 |
| D、将燃着的木条伸入集气瓶中,火焰立即熄灭,证明瓶内气体已经收集满 |
使用“石头纸”(一种不用木材、不用水的环保纸,降解后为尘土,无毒害)以碳酸钙为主要原料制作成便签和文件袋,以实现“低碳”理念.相关说法不正确的是( )
| A、“石头纸”是混合物 |
| B、主要原料碳酸钙属于盐类化合物 |
| C、这种举措旨在将“低碳”、“环保”融入我们生活的一点一滴 |
| D、这种纸容易撕开、不防水 |
下列实验操作正确的是( )
A、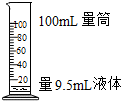 |
B、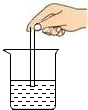 |
C、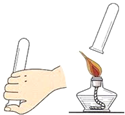 |
D、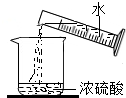 |
2012年4月15日,央视曝光河北一些企业生产的药用胶囊里重金属铬(Cr)超标,即震惊全国的“毒胶囊”事件.已知铬原子核内有24个质子,铬元素的相对原子质量为52,下列有关铬元素的说法中正确的是( )
| A、铬原子的核外电子数为28 |
| B、铬原子呈电中性 |
| C、铬原子中质子数=中子数 |
| D、铬元素的原子序数是52 |
下图所示实验操作中,正确的是( )
A、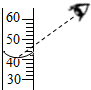 读取液体体积 |
B、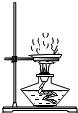 蒸发氯化钠溶液 |
C、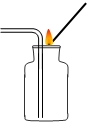 二氧化碳验满 |
D、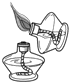 点燃酒精灯 |
下列物质的变化,不能通过一步化学反应实现的是( )
| A、SO3→Na2SO4 |
| B、MgSO4→Mg(OH)2 |
| C、Cu(OH)2→CuCl2 |
| D、KN03→K2SO4 |
下列操作中,不正确的是( )
| A、用胶头滴管向试管中滴加液体时,把滴管伸人试管内 |
| B、称量物体时,物体放托盘天平左盘,砝码放右盘 |
| C、在实验室里制取气体时,应先检查装置气密性 |
| D、为了安全,给试管里的液体加热时,试管口不能朝着有人的方向 |
 小红同学学习了物质、元素、分子、原子、离子五个概念之后,将它的关系总结如图.请你列举具体实例说明它们之间的关系(写出三点)
小红同学学习了物质、元素、分子、原子、离子五个概念之后,将它的关系总结如图.请你列举具体实例说明它们之间的关系(写出三点)