题目内容
12.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂,因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想①可能是CaCl2和Ca(OH)2;猜想②可能只有CaCl2;猜想③CaCl2、HCl.
【查阅资料】氯化钙溶液呈中性
【进行实验】
| 实验步骤 | 实验现象 | 结论 |
| 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液 | 酚酞溶液没有变色 | 猜想①错误 |
| 取少量烧杯内溶液于另一支试管中,加入几滴紫色的石蕊试液 | 石蕊试液变红色 | 猜想③正确 |
【拓展】对于没有明显现象的化学变化,可以从反应物被消耗和相应生成物出现两个方面甲乙证明,对于本题涉及的实验,试从反应物是否被消耗的角度再设计两种方案证明反应确实发生了.
| 实验操作 | 预期实验现象 |
| 在石灰水中加入锌粒,然后逐渐加入稀盐酸 | 如果一段时间后锌粒表面有气泡冒出 |
| 在石灰水中加入几小块石灰石,然后逐渐加入稀盐酸 | 如果一段时间后石灰石表面有气泡冒出 |
分析 (1)根据氢氧化钙和盐酸反应生成了氯化钙和水写出反应的方程式;
(2)猜想③根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;
【实验探究】
Ⅰ根据酚酞遇碱变红来进行解答;
Ⅱ根据盐酸的化学性质分析;
【反思】
根据废液呈酸性,以及盐酸的性质进行分析,但注意不能引进其它的金属离子.
【拓展】根据盐酸的性质进行分析.
解答 解:
(1)氢氧化钙和盐酸反应生成了氯化钙和水,因此反应的方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;
(2)猜想:反应可能是恰好反应,只有氯化钙、也可能是一种物质完全反应,另一种物质有剩余,若氢氧化钙过量,则含有氢氧化钙和氯化钙;若盐酸过量,则含有盐酸和氯化钙;
【实验探究】Ⅰ因为酚酞遇碱会变红色,无色酚酞溶液不变色,说明反应后的溶液不呈碱性.而猜想①中含有Ca(OH)2,溶液应呈碱性,所以排除猜想①;
Ⅱ根据盐酸的化学性质可设计实验如下:
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液 | 酚酞溶液没有变色 | 猜想①错误 |
| 取少量烧杯内溶液于另一支试管中,加入 几滴紫色的石蕊试液 | 石蕊试液变红色 | 猜想③正确 |
废液呈酸性,会腐蚀铁质下水管(或污染水源);除去溶液中的盐酸可用适量的碳酸钙,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳.
【拓展】由于当酸与其他物质反应时,酸碱中和会优先进行,所以从反应物是否被消耗的角度设计实验,可以在石灰水中加入锌粒(或几小块石灰石),然后逐渐加入稀盐酸,如果一段时间后锌粒(或石灰石)表面有气泡冒出,说明进行了反应.
故答案为:
(1)Ca(OH)2+2HCl═CaCl2+2H2O
(2)【猜想与假设】CaCl2、HCl
【实验探究】
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液 | 酚酞溶液没有变色 | 猜想①错误 |
| 取少量烧杯内溶液于另一支试管中,加入 几滴紫色的石蕊试液 | 石蕊试液变红色 | 猜想③正确 |
【反思与拓展】CaCO3.
| 实验操作 | 预期实验现象 |
| 在石灰水中加入锌粒,然后逐渐加入稀盐酸 | 如果一段时间后锌粒表面有气泡冒出 |
| 在石灰水中加入几小块石灰石,然后逐渐加入稀盐酸 | 如果一段时间后石灰石表面有气泡冒出 |
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手.

练习册系列答案
相关题目
7.下列实验操作正确的是( )
| A. | 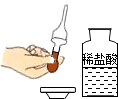 吸取液体 | B. | 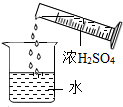 稀释浓硫酸 | C. | 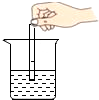 测定溶液的pH | D. | 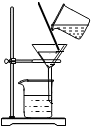 过滤 |
17.舌尖上的化学.下列食品制作过程中,不涉及化学变化的是( )
| A. | 葡萄酿酒 | B. | 柴火烧鹅 | C. | 鲜果榨汁 | D. | 猪骨煲汤 |
2.如图是甲、乙、丙三种固体物质的溶解度曲线.下列有关说法错误的是( )
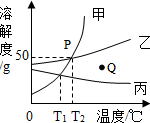

| A. | 丙物质的溶解度随温度的升高而降低 | |
| B. | T1℃时三种物质的饱和溶液,乙的溶质质量分数最大 | |
| C. | P点表示T2℃时甲、乙的饱和溶液中,溶质质量分数均为50% | |
| D. | 甲中混有少量乙时通常可以用冷却甲的热饱和溶液方法提纯甲 |