题目内容
8.若金属锰在金属活动性顺序表中位于铝和锌之间,则下列反应不正确的是( )| A. | Mn+H2SO4═MnSO4+H2 | B. | Mg+MnSO4═MgSO4+Mn | ||
| C. | Fe+MnSO4═FeSO4+Mn | D. | Mn+CuSO4═MnSO4+Cu |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来;据此进行分析判断
解答 解:A、金属锰在金属活动性顺序中位于铝和锌之间,铝、锌是氢之前的金属,则锰排在氢的前面,能和盐酸发生置换反应,故A正确;
B、金属锰在金属活动性顺序中位于铝和锌之间,则锰的活动性比镁弱,所以镁能与MnSO4溶液发生置换反应,故B正确;
C、金属锰在金属活动性顺序中位于铝和锌之间,锰的活动性比铁强,所以铁不能和MnSO4溶液发生置换反应,故C不正确;
D、金属锰在金属活动性顺序中位于铝和锌之间,则锰排在铜的前面,能与CuSO4溶液发生置换反应,故D正确.
故选C.
点评 本题难度不是很大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
相关题目
3.下列粒子的化学性质与镁原子  最相似的是( )
最相似的是( )
 最相似的是( )
最相似的是( )| A. |  | B. |  | C. |  | D. |  |

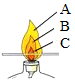 (1)点燃蜡烛,顶端熔化成液体,形成的火焰分三层,分别是外焰、内焰和焰心.
(1)点燃蜡烛,顶端熔化成液体,形成的火焰分三层,分别是外焰、内焰和焰心. 燃烧与我们的生活与社会的发展有着密切的联系.
燃烧与我们的生活与社会的发展有着密切的联系.