题目内容
把
20g一氧化碳和二氧化碳的混合气体,通过灼热的氧化铜,完全反应后气体质量变为28g.求原混合气体中二氧化碳的质量是多少克.
答案:
解析:
解析:
|
答:原混合气中含 CO2的质量为6g解法 1:设原混合气中CO2的质量为x,则CO的质量为(20g-x),则由CO生成的CO2质量为(28g-x)CO+CuO 28 44 20g-x 28g-x
解法 2:差量法设原混合气中 CO的质量为xCO+CuO 28 44 16由(44-28)求得 x (28-20)g
原混合气中含 CO2(20g-14g)=6g思路分析:混合气通过灼热的 CuO时,CO和CuO发生反应,CO2与CuO不发生反应.反应后的28g气体为CO2气,这些CO2气有一部分来自原混合气中的CO2,另一部分由CO和CuO反应所生成.原混合气(含CO和CO2)为20g,反应后的气体(只含CO2)为28g,气体质量增加的原因是CO结合CuO中的氧生成CO2所致.故气体增加的质量应是CuO中所含氧元素的质量,也是CO在反应中结合的氧元素的质量.本题可用差量法求解,也可根据化学方程式或关系式求解. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
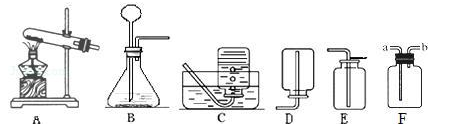
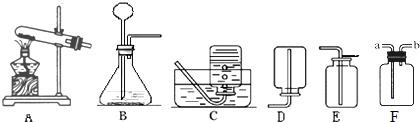
根据下图所示装置回答问题:
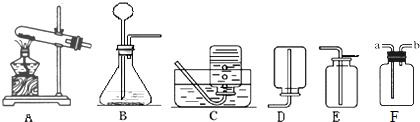
(1)实验室用大理石和稀盐酸反应制取二氧化碳,应选用的装置是 ,请写出该反应的化学方程式: .
(2)实验室用A装置加热高锰酸钾来制取氧气,需要改进的是 ,反应的化学方程式为 .下列反应可使用A装置进行实验的是(填序号) .
①过氧化氢溶液和二氧化锰制氧气; ②一氧化碳还原氧化铁; ③木炭还原氧化铜
(3)装置F可用来收集气体,还具有其他用途,如在F瓶中装入 ,可用来干燥某些气体.若用F收集氧气并测量制得氧气的体积,需在瓶内先装满水,气体从 (填“a”或“b”)处导管通入,并需要补充的一种玻璃仪器是 .
(4)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
试计算该稀盐酸的溶质质量分数.

(1)实验室用大理石和稀盐酸反应制取二氧化碳,应选用的装置是
(2)实验室用A装置加热高锰酸钾来制取氧气,需要改进的是
①过氧化氢溶液和二氧化锰制氧气; ②一氧化碳还原氧化铁; ③木炭还原氧化铜
(3)装置F可用来收集气体,还具有其他用途,如在F瓶中装入
(4)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加入5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |
根据下图所示装置回答问题:

(1)实验室用大理石和稀盐酸反应制取二氧化碳,应选用的装置是________,请写出该反应的化学方程式:________.
(2)实验室用A装置加热高锰酸钾来制取氧气,需要改进的是________,反应的化学方程式为________.下列反应可使用A装置进行实验的是(填序号)________.
①过氧化氢溶液和二氧化锰制氧气; ②一氧化碳还原氧化铁; ③木炭还原氧化铜
(3)装置F可用来收集气体,还具有其他用途,如在F瓶中装入________,可用来干燥某些气体.若用F收集氧气并测量制得氧气的体积,需在瓶内先装满水,气体从________(填“a”或“b”)处导管通入,并需要补充的一种玻璃仪器是________.
(4)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加入5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |