题目内容
8.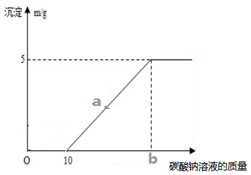 某科学兴趣小组同学为测定大理石和盐酸反应后的废液成分,取50克该废液逐滴加入碳酸钠溶液,根据实验测定的数据绘出右如图,其中纵坐标表示沉淀的质量,横坐标表示碳酸钠溶液的质量.请回答:
某科学兴趣小组同学为测定大理石和盐酸反应后的废液成分,取50克该废液逐滴加入碳酸钠溶液,根据实验测定的数据绘出右如图,其中纵坐标表示沉淀的质量,横坐标表示碳酸钠溶液的质量.请回答:(1)分析图象可知,开始加入碳酸钠溶液至10克,没有产生沉淀的原因碳酸钠先和废液中的盐酸反应.
(2)如图在a点时溶液中的溶质的成分为NaCl、CaCl2
(3)废液中氯化钙的质量分数为多少?
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,氯化钙和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,根据提供的信息和数据可以进行相关方面的计算和判断.
解答 解:(1)分析图象可知,开始加入碳酸钠溶液至10g,没有产生沉淀,是因为废液中含有盐酸,加入碳酸钠溶液时,碳酸钠先和废液中的盐酸反应生成氯化钠、水和二氧化碳.
故填:碳酸钠先和废液中的盐酸反应.
(2)如图在a点时溶液中的溶质的成分有反应生成的氯化钠和没有反应的氯化钙.
故填:NaCl、CaCl2.
(3)设废液中氯化钙质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
111 100
x 5g
$\frac{111}{x}$=$\frac{100}{5g}$,
x=5.55g,
废液中氯化钙的质量分数为:$\frac{5.55g}{50g}$×100%=11.1%,
答:废液中氯化钙的质量分数为11.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
19. 如图是小俊用手势OK表示初中常见化学反应中生成二氧化碳的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成二氧化碳(如图中的H2CO3、O2),则物质X一定不可能是( )
如图是小俊用手势OK表示初中常见化学反应中生成二氧化碳的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成二氧化碳(如图中的H2CO3、O2),则物质X一定不可能是( )
 如图是小俊用手势OK表示初中常见化学反应中生成二氧化碳的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成二氧化碳(如图中的H2CO3、O2),则物质X一定不可能是( )
如图是小俊用手势OK表示初中常见化学反应中生成二氧化碳的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成二氧化碳(如图中的H2CO3、O2),则物质X一定不可能是( )| A. | CH4 | B. | CaCO3 | C. | C | D. | CuO |
13.下列各图所示装置的气密性检查中,漏气的是( )
| A. | 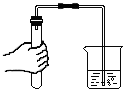 | B. | 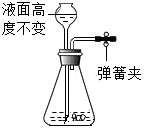 | ||
| C. | 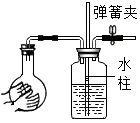 | D. | 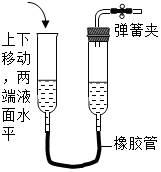 |
17.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别氢氧化钠溶液和氢氧化钙溶液 | 通入二氧化碳气体 |
| B | 除去CO2中少量的CO | 点燃 |
| C | 检验一瓶气体是否为CO2 | 将燃着的木条伸入瓶中 |
| D | 除去FeSO4中的CuSO4 | 加入过量的Zn,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
 化学与人类生活息息相关.请回答下列问题.
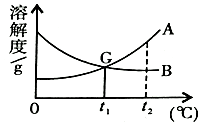
化学与人类生活息息相关.请回答下列问题. 某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图.
某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图.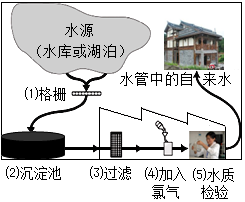 城市住宅饮用水处理过程如图.
城市住宅饮用水处理过程如图. 教材中说到治病所用的药品,其实就是化学药品,用于治病,保护身体健康.如图是一种常见的止血药氨基乙酸的部分信息.请根据信息回答问题:
教材中说到治病所用的药品,其实就是化学药品,用于治病,保护身体健康.如图是一种常见的止血药氨基乙酸的部分信息.请根据信息回答问题: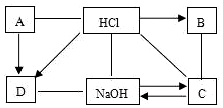 如图是六种物质之间的转化关系.用“一”表示两种物质之间能发生反应,用“→”表示一种物质可以转化为另一种物质.其中A、B分别是三氧化二铁和氯化钙溶液中的一种,C是一种盐溶液,D常用于灭火(部分反应、转化关系已省略,初中知识范围 内).请回答下列问题:
如图是六种物质之间的转化关系.用“一”表示两种物质之间能发生反应,用“→”表示一种物质可以转化为另一种物质.其中A、B分别是三氧化二铁和氯化钙溶液中的一种,C是一种盐溶液,D常用于灭火(部分反应、转化关系已省略,初中知识范围 内).请回答下列问题: