题目内容
CaCO3和MgCO3的混合物9g,与足量的盐酸反应,生成CO2的质量可能是( )
【答案】分析:假定9g物质全部是碳酸钙或碳酸镁,根据化学方程式计算出生成二氧化碳的质量,得到的数据一个是生成二氧化碳质量的最大值,一个是生成二氧化碳质量的最小值,因此生成二氧化碳的质量应介于二者之间.
解答:解:设9g物质全部为碳酸钙时生成二氧化碳的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
9g x
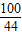 =
=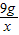 ,x=3.96g
,x=3.96g
设9g物质全部为碳酸钙时生成二氧化碳的质量为y.
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
9g y
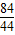 =
= ,y=4.71g
,y=4.71g
通过以上计算可知生成二氧化碳质量应在3.96g与4.71g之间.
故选B.
点评:本题主要考查有关化学方程式的计算,难度较大.关键是找到生成二氧化碳的质量介于9g物质全部为碳酸镁和9g物质全部为碳酸钙时生成二氧化碳的质量之间.
解答:解:设9g物质全部为碳酸钙时生成二氧化碳的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
9g x
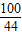 =
=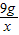 ,x=3.96g
,x=3.96g设9g物质全部为碳酸钙时生成二氧化碳的质量为y.
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
9g y
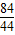 =
= ,y=4.71g
,y=4.71g通过以上计算可知生成二氧化碳质量应在3.96g与4.71g之间.
故选B.
点评:本题主要考查有关化学方程式的计算,难度较大.关键是找到生成二氧化碳的质量介于9g物质全部为碳酸镁和9g物质全部为碳酸钙时生成二氧化碳的质量之间.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
CaCO3和MgCO3的混合物9g,与足量的盐酸反应,生成CO2的质量可能是( )
| A、3.8g | B、4.4g | C、4.8g | D、5.2g |