题目内容
17.在200克溶质质量分数为10%的氯化钠溶液中,(1)倒出100克溶液,这时原溶液的质量分数是多少?倒出溶液的质量分数是多少?(2)剩余溶液中再溶解10克氯化钠,这时溶液的溶质质量分数是多少?
(3)再加人10克水,这时溶液中溶质质量分数是多少?
(4)再加入100克质量分数为10%的氯化钠溶液这时溶液中溶质的质量分数是多少?
分析 根据溶液具有均一性,结合溶质质量分数=$\frac{溶质质量}{溶液质量}×$100%,溶质质量=溶液质量×溶质的质量分数,溶液稀释前后溶质的质量不变,进行分析解答.
解答 解:(1)溶液具有均一性,在200克溶质质量分数为10%的氯化钠溶液中,倒出100克溶液,这时原溶液的质量分数是10%,倒出溶液的质量分数是10%.
(2)剩余溶液中再溶解10克氯化钠,这时溶液的溶质质量分数是$\frac{100g×10%+10g}{100g+10g}$×100%≈18.2%.
(3)溶液稀释前后溶质的质量不变,再加人10克水,这时溶液中溶质质量分数是$\frac{100g×10%+10g}{100g+10g+10g}$×100%≈16.7%.
(4)再加入100克质量分数为10%的氯化钠溶液,这时溶液中溶质的质量分数是$\frac{100g×10%+10g+100g×10%}{100g+10g+10g+100g}$×100%≈13.6%.
答:(1)原溶液的质量分数是10%,倒出溶液的质量分数是10%;
(2)这时溶液的溶质质量分数是18.2%;
(3)这时溶液的溶质质量分数是16.7%;
(4)这时溶液的溶质质量分数是13.6%.
点评 本题难度不大,掌握溶质质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变等是正确解答本题的关键.

练习册系列答案
相关题目
7.下列化学方程式正确的是(反应条件忽略)( )
| A. | C+2S═CS2 | B. | AgNO3+CaCl2═AgCl↓+CaNO3 | ||
| C. | 2Al+3O2═2Al2O3 | D. | NH4HCO3(固体)═NH3+H2O+CO2 |
5.已知反应2A+3B=C,每次取10g反应物进行实验,数据如下表,则第三次实验中x:y可能是( )
A.2:1 B.3:1 C.3:2 D.7:3.
| A/g | B/g | C/g | |
| 第一次 | 8 | 2 | 6 |
| 第二次 | 4 | 6 | 6 |
| 第三次 | X | Y | 9 |
10.小强同学用量筒量取液体,将量筒放好后,先俯视量筒内液体凹液面的最低处,读数为21mL,倒出部分液体后,仰视凹液面的最低处,读数为8mL,则该同学实际倒出液体的体积( )
| A. | 大于13mL | B. | 等于13mL | C. | 小于13mL | D. | 无法判断 |
 碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题:
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题: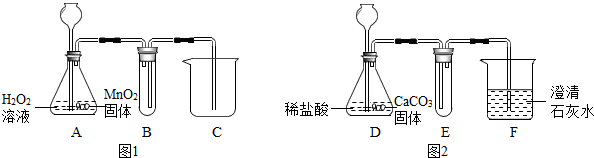
 某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置图进行过滤,请回答下列问题:
某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置图进行过滤,请回答下列问题: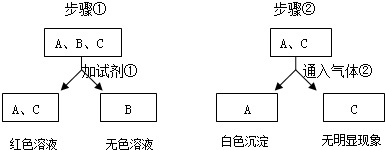 现有盐酸、氢氧化钠、氢氧化钙三瓶遗失标签的溶液,为了鉴别这些溶液,将它们编号为A、B、C,并按下图步骤进行实验,观察到以下现象:
现有盐酸、氢氧化钠、氢氧化钙三瓶遗失标签的溶液,为了鉴别这些溶液,将它们编号为A、B、C,并按下图步骤进行实验,观察到以下现象: