题目内容
16.实验室可用加热氯酸钾与二氧化锰的混合物制取氧气,现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g.求:①反应生成氧气的质量是多少?
②原混合物中氯酸钾的质量是多少?
分析 根据质量守恒定律分析生成氧气的质量,根据化学方程式计算混合物中氯酸钾的质量.
解答 解:(1)根据质量守恒定律,反应生成氧气的质量为:30g-20.4g=9.6g;
(2)设原混合物中氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 9.6g
$\frac{245}{x}$=$\frac{96}{9.6g}$
x=24.5g
答:反应生成氧气的质量是9.6g;
原混合物中氯酸钾的质量是24.5g.
故答案为:①9.6克;
②24.5克.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式、化学方程式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列有关“化学之最”的叙述中,错误的是( )
| A. | 相对分子质量最小的化合物是水 | B. | 相对分子质量最小的气体是氢气 | ||
| C. | 天然存在最硬的物质是金刚石 | D. | 地壳中含量最多的元素是铝元素 |
8.下列过程中,只发生了化学变化的是( )
| A. | 酒精挥发 | B. | 酒精燃烧 | C. | 冰雪融化 | D. | 矿石粉碎 |
5. 认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
(1)在海水的大量元素中,含有的金属元素有4种
(2)用人体中含量前四位元素可以组成多种物质,请结合所学写出符合下列要求的物质各一种:①单质氧气,②氧化物水
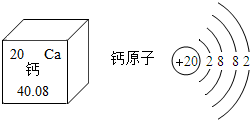
(3)如图所示,是钙元素在元素周期表中想相关信息.请回答:
①钙元素的原子序数是20
②钙原子易失(填“得”或“失”)电子,形成钙离子,钙离子的符号是Ca2+
③青少年缺钙易引起A(填序号)
A、佝偻病 B、贫血病 C、甲状腺肿大.
 认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:| 含量次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 人体中 | H | O | C | N | Na | Ca | P | S | K | Cl |
| 海水中 | H | O | Na | Cl | Mg | S | K | Ca | C | N |
(2)用人体中含量前四位元素可以组成多种物质,请结合所学写出符合下列要求的物质各一种:①单质氧气,②氧化物水
(3)如图所示,是钙元素在元素周期表中想相关信息.请回答:
①钙元素的原子序数是20
②钙原子易失(填“得”或“失”)电子,形成钙离子,钙离子的符号是Ca2+
③青少年缺钙易引起A(填序号)
A、佝偻病 B、贫血病 C、甲状腺肿大.
12.铝在一百多年里产量得到大幅度的提高,并被广泛地使用,原因之一就是铝的抗腐蚀性能好.铝具有良好抗腐蚀性能的原因是( )
| A. | 铝的化学性质不活泼 | |
| B. | 铝不与酸、氧气等物质反应 | |
| C. | 铝常温下不与氧气反应 | |
| D. | 铝表面形成一层致密的氧化铝保护膜 |