题目内容
2.原子是化学变化中的最小粒子,但不是不可分割的实心球体.原子由居于原子中心的带正电的原子核和带负电的电子构成.(1)在原子中,核电荷数=质子数=核外电子数,因此原子不显电性.
(2)同种原子中,中子数不一定等于质子数.
(3)不是所有原子都有中子,如氢原子.
(4)相对原子质量(整数)=质子数+中子数.
分析 根据原子的构成、微粒的电性以及原子中各种微粒的数目关系分析回答.
解答 解:原子是化学变化中的最小粒子,但不是不可分割的实心球体.原子由居于原子中心的带正电的原子核和带负电的电子构成.
(1)在原子中,核电荷数=质子数=核外电子数,因此原子不显电性.
(2)同种原子中,中子数不一定等于质子数.
(3)不是所有原子都有中子,如氢原子.
(4)相对原子质量(整数)=质子数+中子数.
故答为:化学,正,原子核,电子.
(1)核电荷,质子.
(2)中子,质子.
(3)中子.
(4)质子,中子.
点评 本题主要考查了原子的定义和构成,难度不大,能正确地理解原子的构成是解答本题的基础.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
10.氧气是我们身边常见的物质,以下有关氧气的叙述正确的是( )
| A. | 物质与氧气发生的反应都是氧化反应 | |
| B. | 鱼、虾等能在水中生存,是由于氧气易溶于水 | |
| C. | 氧气能支持燃烧,可作燃料 | |
| D. | 带火星的木条一定能在含有氧气的集气瓶中燃烧 |
17.在O2、SO2、MnO2三种物质中,下列叙述正确的是( )
| A. | 都含有一个氧分子 | B. | 都含氧元素 | ||
| C. | 都是氧化物 | D. | 都是化合物 |
7.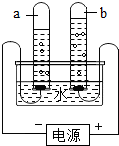 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
(1)通电后电极上出现气泡,并汇集到试管上端.正极产生的气体能支持燃烧,负极产生的气体能燃烧.则正极产生的气体是氧气,负极产生的气体是氢气.
(2)实验时常在水中加入硫酸或氢氧化钠,目的是增强水的导电性.
(3)在某次电解水的实验中加入了少量的氢氧化钠溶液,测得了分别与电源正负两极相连的阳、阴两极上产生的气体体积的实验数据如表:
仔细分析以上实验数据,1~3分钟内阴、阳两极生成的气体体积之比大于2:1,可能的原因是氧气比氢气更易溶于水(写一条),从第4分钟开始每分钟内阴、阳两极生成的气体体积之比约为2:1,可能的原因是溶解在水中的氧气和氢气都达到了饱和,不再继续溶解了.
 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:(1)通电后电极上出现气泡,并汇集到试管上端.正极产生的气体能支持燃烧,负极产生的气体能燃烧.则正极产生的气体是氧气,负极产生的气体是氢气.
(2)实验时常在水中加入硫酸或氢氧化钠,目的是增强水的导电性.
(3)在某次电解水的实验中加入了少量的氢氧化钠溶液,测得了分别与电源正负两极相连的阳、阴两极上产生的气体体积的实验数据如表:
时间/分钟 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 负极生成气体体积 (cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 正极生成气体体积 (cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
11.某些盐在溶液中结晶时,析出的晶体是结晶水合物.下表记录了t℃的4份相同的硫酸铜溶液中加入的无水硫酸铜的质量以及析出的硫酸铜晶体(CuSO4•5H2O)的质量(温度维持不变)的实验数据:
当加入a g(5<a<11)无水硫酸铜时,析出硫酸铜晶体的质量(g)为( )
| 硫酸铜溶液 | ① | ② | ③ | ④ |
| 加入的无水硫酸铜(g) | 2.50 | 5.00 | 8.00 | 11.0 |
| 析出的硫酸铜晶体(g) | 0.10 | 4.60 | 10.0 | 15.4 |
| A. | 1.8a-4.4 | B. | 1.8a-8 | C. | 1.8a-4.6 | D. | 1.8a-0.1 |
12.下列化学方程式书写正确的是( )
| A. | 2H2O$\frac{\underline{\;点燃\;}}{\;}$2H2↑+O2↑ | B. | H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | ||
| C. | Fe+O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | D. | S+O2↑$\frac{\underline{\;点燃\;}}{\;}$SO2↑ |
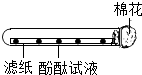 如图是有关分子性质的实验:在滤纸条上每隔2厘米处滴一滴无色酚酞试液,将滤纸条放入试管中,并在试管口塞上一团棉花.用滴管吸取浓氨水,将它滴在棉花上:
如图是有关分子性质的实验:在滤纸条上每隔2厘米处滴一滴无色酚酞试液,将滤纸条放入试管中,并在试管口塞上一团棉花.用滴管吸取浓氨水,将它滴在棉花上: