题目内容
1.漂白粉在空气中发生反应的化学方程式是Ca(ClO)2+X+H2O═CaCO3↓+2HClO,则X的化学式是( )| A. | CO | B. | CO2 | C. | CH4 | D. | O2 |
分析 根据质量守恒定律可知:反应前后元素种类不变,原子个数不变.由以上依据可推出X的化学式.
解答 解:根据质量守恒定律可知,反应前后元素的种类不变,原子个数不变,由Ca(ClO)2+X+H2O=CaCO3↓+2HClO可知,反应前氯原子有2个,钙原子有1个,氧原子有3个,氢原子2个,而反应后氯原子有2个,钙原子有1个氧原子有5个,氢原子2个,碳原子1个,所以X的化学每个X微粒中含有1个碳原子和2个氧原子,是二氧化碳,化学式为:CO2.
故选:B.
点评 解答本题要掌握质量守恒定律的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
2.下列有关硫酸的说法,正确的是( )
| A. | 打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾 | |
| B. | 浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%-5%的碳酸氢钠溶液 | |
| C. | 实验室用稀硫酸和石灰石制取二氧化碳 | |
| D. | 把铜片放入稀硫酸中,产生大量气泡 |
9.化学影响着社会的发展和我们的生活质量.以下认识不正确的是( )
| A. | 吸附能使硬水变为软水 | |
| B. | 用纯碱可除去面团发酵产生的酸 | |
| C. | 不能用工业酒精勾兑饮用酒 | |
| D. | 回收废旧金属既节约金属资源,又减少环境污染 |
13.下列说法中正确的是( )
| A. | 具有相同质子数的微粒一定属于同一种元素 | |
| B. | 不饱和溶液变成饱和溶液后溶质的质量分数可能不变 | |
| C. | 分子可以再分,而原子不能再分 | |
| D. | 由不同种元素组成的物质一定是化合物 |
10.已知木炭还原氧气铜实验中会发生如下反应:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
某化学兴趣小组做该实验时所得产物是暗红色固体,没有观察到紫红色固体,于是他们对反应产物(假设反应物已完全反应)作如下实验探究:
信息提示:1氧化亚铜(Cu2O)为砖红色固体;
2Cu2O+H2SO4═CuSO4+Cu+H2O;
3碱石灰为氧化钙和氢氧化钠的混合物
[实验一]探究反应产物的成分
兴趣小组的同学讨论交流后,认为暗红色固体除了有铜外,还可能含有Cu2O(其中Cu的化合价是+1).为此,他们设计了以下实验:取少量暗红色固体于试管中,加入少量稀硫酸,振荡,如果观察到溶液由无色变为蓝色,说明暗红色固体中含有Cu2O.
[实验二]测定产物中Cu2O的含量
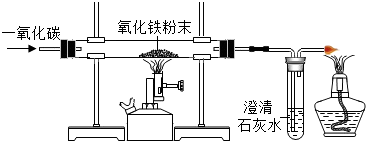
原理:Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O,称取一定质量的固体产物,用下图装置进行实验(固定装置略去),通过测定反应前后装置d的质量达到实验目的.

(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸易挥发,挥发出的氯化氢能被碱石灰吸收,影响测定结果;写出装置a中反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)点燃酒精灯前,要先打开弹簧夹K1,关闭弹簧夹K2,对装置c通一会儿氢气,目的是:把装置中的空气排出去,以免加热时发生爆炸.
(3)装置b的作用是干燥氢气;装置d的质量在反应前后会发生改变,是因为它吸收了反应生成的水.
(4)反应前后,测得装置d的质量如表:
根据测得数据可行:产物中Cu2O的质量为1.44g.
(5)如果没有接上装置e,则实验得出结果将偏大(选填“偏大”、“偏小”或“不变”).
某化学兴趣小组做该实验时所得产物是暗红色固体,没有观察到紫红色固体,于是他们对反应产物(假设反应物已完全反应)作如下实验探究:
信息提示:1氧化亚铜(Cu2O)为砖红色固体;
2Cu2O+H2SO4═CuSO4+Cu+H2O;
3碱石灰为氧化钙和氢氧化钠的混合物
[实验一]探究反应产物的成分
兴趣小组的同学讨论交流后,认为暗红色固体除了有铜外,还可能含有Cu2O(其中Cu的化合价是+1).为此,他们设计了以下实验:取少量暗红色固体于试管中,加入少量稀硫酸,振荡,如果观察到溶液由无色变为蓝色,说明暗红色固体中含有Cu2O.
[实验二]测定产物中Cu2O的含量
原理:Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O,称取一定质量的固体产物,用下图装置进行实验(固定装置略去),通过测定反应前后装置d的质量达到实验目的.

(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸易挥发,挥发出的氯化氢能被碱石灰吸收,影响测定结果;写出装置a中反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)点燃酒精灯前,要先打开弹簧夹K1,关闭弹簧夹K2,对装置c通一会儿氢气,目的是:把装置中的空气排出去,以免加热时发生爆炸.
(3)装置b的作用是干燥氢气;装置d的质量在反应前后会发生改变,是因为它吸收了反应生成的水.
(4)反应前后,测得装置d的质量如表:
| 反应前 | 反应后 | |
| 装置d(含药品)的质量/g | 100.00 | 100.18 |
(5)如果没有接上装置e,则实验得出结果将偏大(选填“偏大”、“偏小”或“不变”).
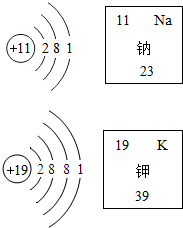 如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.
如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.