题目内容
16.在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入过量的铁粉,充分反应过程中,获得或剩余金属的质量与所加铁的质量的关系正确的是( )| A. |  | B. | 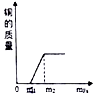 | C. | 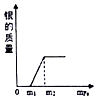 | D. | 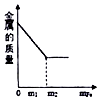 |
分析 根据三种金属活动性由强到弱的关系铁>铜>银,在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,铁粉首先与硝酸银反应得到银,待硝酸银完全反应后开始与硝酸铜发生反应置换出铜.
解答 解:A、随着反应进行铁的质量会逐渐减小,最后不变,故A错误;
B、由于所加入的铁粉首先与硝酸银反应,因此开始加入铁粉时得到铜的质量为0;待硝酸银完全反应后才开始有铜出现,所得铜的质量不断增加,直到硝酸铜完全反应铜的质量不再改变;故B正确;
C、由于所加入的铁粉首先与硝酸银反应,因此开始加入铁粉时得到银的质量为0;随着反应进行有银出现,直到硝酸银完全反应银的质量不再改变;故C错误;
D、铁与硝酸银、硝酸铜的反应过程中,金属的质量都不断增加,由于银的相对原子质量比铜大,所以与硝酸银反应阶段金属质量增加的速度比与硝酸铜反应时要更大些;两种物质完全反应后所得到的金属的质量不再改变;故D错误;
故选B.
点评 根据曲线的纵横坐标轴的说明,判断曲线所表示的变化关系,此是正确答题的根本.同时注意金属反应的优先原则的应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.在构成原子的粒子中数目相同的是( )
| A. | 质子数和中子数 | B. | 质子数和电子数 | C. | 中子数和电子数 | D. | 都不相同 |
11.下列变化中,属于化学变化的是( )
| A. | 雪熔化 | B. | 水结冰 | C. | 冰升华 | D. | 水电解 |
1.某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42-的离子个数比为( )
| A. | 1:2 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
8.下列判断结果正确的是( )
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
| A. | 只有(1)(3)正确 | B. | 只有(2)(3)正确 | C. | 只有(3)(5)(6)正确 | D. | 都不正确 |
6.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物:甲烷、乙醇、乙酸 | |
| B. | 复合肥料:尿素[CO(NH2)2]、硝酸钾、磷酸氢二铵[NH4H2PO4] | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 合成材料:合金、合成橡胶、合成纤维 |

 如图表示NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之问可以发生化学反应.
如图表示NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之问可以发生化学反应.