题目内容
7.化学课上老师向盛有NaOH溶液的试管中滴入2-3滴无色酚酞试液,振荡溶液呈红色.提出问题:是什么微粒使无色酚酞变红?
查阅资料:NaOH溶液中主要存在H2O、OH-、Na+三种粒子.
猜想:①水分子使无色酚酞变红;
②Na+使无色酚酞变红;
③OH-使无色酚酞变红.
实验验证:
| 实验操作 | 现象 | 结论 |
| 实验一:分别向盛有NaOH溶液和蒸馏水的试管中滴入2-3滴无色酚酞试液 | NaOH溶液中滴入酚酞后变红,蒸馏水中滴入酚酞后无现象. | 猜想①不成立. |
| 实验二:分别向盛有NaOH溶液和NaCl溶液的试管中滴入2-3滴无色酚酞试液 | NaOH溶液中滴入酚酞后变红,NaCl溶液中滴入酚酞后无现象. | 猜想②不成立. |
| 实验三:分别向盛有NaOH溶液和石灰水的试管中滴入2-3滴无色酚酞试液 | 两支试管中滴入酚酞后均变红. | 猜想③成立. |
分析 猜想、根据氢氧化钠溶液中含有的粒子进行猜想;
实验验证:根据固定变量法选择物质探究能使酚酞变色的粒子.
解答 解:猜想:由于NaOH溶液中主要存在H2O、OH-、Na+三种粒子.所以,猜想③是:OH-使无色酚酞变红.
实验验证:为了探究水分子、钠离子、氢氧根离子是否是酚酞试液变色,可以用蒸馏水、氯化钠、氢氧化钙进行试验,实验如下:
| 实验操作 | 现象 | 结论 |
| 实验一:分别向盛有NaOH溶液和蒸馏水的试管中滴入2-3滴无色酚酞试液 | NaOH溶液中滴入酚酞后变红,蒸馏水中滴入酚酞后无现象. | 猜想①不成立. |
| 实验二:分别向盛有NaOH溶液和NaCl溶液的试管中滴入2-3滴无色酚酞试液 | NaOH溶液中滴入酚酞后变红,NaCl溶液中滴入酚酞后无现象. | 猜想②不成立. |
| 实验三:分别向盛有NaOH溶液和石灰水的试管中滴入2-3滴无色酚酞试液 | 两支试管中滴入酚酞后均 变红. | 猜想③成立 |
| 实验操作 | 现象 | 结论 |
| ① | ||
| 分别向盛有NaOH溶液和NaCl溶液的试管中滴入2-3滴无色酚酞试液 | NaOH溶液中滴入酚酞后变红,NaCl溶液中滴入酚酞后无现象. | |
| 变红 |
点评 本题主要探究了氢氧化钠溶液中能使酚酞变色的粒子,会应用固定变量法探究物质性质的方法是解答本题的基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.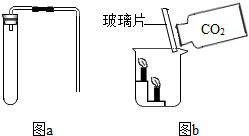 化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.
化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.
【制取与性质】
如图a,检查装置的气密性,操作为先把导管的一端放入水中,然后两手紧握试管的外壁,观察到导管口有气泡冒出.然后加入药品,固定装置,制取CO2,有关化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
如图b,现象为下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明CO2的性质是二氧化碳的密度比空气的密度大,二氧化碳既不能燃烧,也不能支持燃烧.
【反思与交流】
(1)制备气体时选择发生装置需考虑的因素有反应物的状态和反应的条件.
(2)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
[提出猜想]除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂.
[完成实验]按下表进行实验:并测定分解温度(分解温度越低,催化效果越好).
[分析数据、得出结论]
(1)由实验①与实验④对比,证明猜想合理.
(2)实验所用的三种金属氧化物,催化效果最好的是MnO2.
[反思]
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证:分别取相同质量的颗粒大小相同的氯酸钾,与颗粒大小不同的二氧化锰混合加热制氧气,颗粒小的反应的速率快_.
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可).催化剂的多少有关,分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,质量多的反应的速率快.
 化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.
化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.【制取与性质】
如图a,检查装置的气密性,操作为先把导管的一端放入水中,然后两手紧握试管的外壁,观察到导管口有气泡冒出.然后加入药品,固定装置,制取CO2,有关化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
如图b,现象为下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明CO2的性质是二氧化碳的密度比空气的密度大,二氧化碳既不能燃烧,也不能支持燃烧.
【反思与交流】
(1)制备气体时选择发生装置需考虑的因素有反应物的状态和反应的条件.
(2)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
[提出猜想]除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂.
[完成实验]按下表进行实验:并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比l:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
(1)由实验①与实验④对比,证明猜想合理.
(2)实验所用的三种金属氧化物,催化效果最好的是MnO2.
[反思]
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证:分别取相同质量的颗粒大小相同的氯酸钾,与颗粒大小不同的二氧化锰混合加热制氧气,颗粒小的反应的速率快_.
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可).催化剂的多少有关,分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,质量多的反应的速率快.
4.除去下列物质中的少量杂质,所用试剂或方法不正确的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | CO | H2 | 通入O2中点燃 |
| B | N2 | O2 | 通过足量灼热的铜丝 |
| C | KNO3溶液 | Ba(NO3)2 | 滴加适量K2SO4溶液,过滤 |
| D | NaCl溶液 | Na2CO3 | 滴加稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
15.(1)硫酸铜与某些物质能发生反应,请写出2个化学方程式和实验现象.
(2)有一瓶溶液pH是4.5,如果要使溶液的pH升高,可以用向溶液中加水或加入显碱性的物质 的方法.
| 化学方程式 | 现 象 | |
| (1)与碱 | ||
| (2)与盐 |
2.下面对某些实验现象的描述,不正确的是( )
| A. | 鸡蛋壳能溶于醋酸,并产生气泡 | |
| B. | CuSO4溶液中滴入氨水,产生蓝色沉淀 | |
| C. | H2还原CuO,固体由黑色变为红色,并有水珠生成 | |
| D. | 铁丝在纯氧中燃烧,火星四射,产生红棕色固体 |
16.下列叙述正确的是( )
| A. | 浓盐酸有挥发性,所以浓硫酸也有挥发性 | |
| B. | pH<6.5的雨水称为酸雨 | |
| C. | 洗涤剂具有乳化作用能除去餐具上的油污 | |
| D. | 碱的溶液能使无色酚酞试液变红色,所以使无色酚酞试液变红色的溶液一定是碱的溶液 |
17.下列合金(括号内的物质是该合金的主要成分),不能被稀盐酸腐蚀的是( )
| A. | 锰钢(铁、锰、碳) | B. | 黄铜(铜、锌) | C. | 18K黄金(金、银、铜) | D. | 硬铝(铝、铜、镁、硅) |
 樱桃是一种人们非常喜爱的水果,图中所列的樱桃营养成分中,能给人体提供能量的是糖类和蛋白质;图中钾和磷是指元素(选填“原子”、“分子”或“元素”)
樱桃是一种人们非常喜爱的水果,图中所列的樱桃营养成分中,能给人体提供能量的是糖类和蛋白质;图中钾和磷是指元素(选填“原子”、“分子”或“元素”)