题目内容
1.某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将6.0g KClO3与2.0g MnO2均匀混合加热
II.将x g KClO3与2.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.II中x的值为6.0.
②乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |
I.本实验中,测量O2体积的装置是C(填编号).
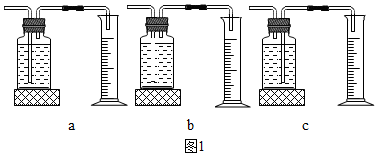
II.实验结论:在相同条件下,双氧水分解得快.
?某同学继续探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
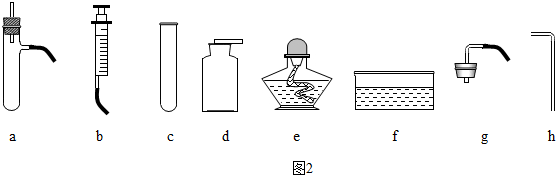
a、他分别向两支试管中加入相同的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
b、将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c、用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
试回答:步骤a中他除了选用试管外还用到上面列出的仪器有fgh(填字母).步骤c的实验目的是证明红砖粉末在反应前后的化学性质没有改变.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来.实验开始没有称量红砖粉末的质量.
分析 ①可采用控制变量法,要控制氯酸钾的质量相等才能比较出二氧化锰和氧化铜的催化效果,据此进行分析解答.
【数据处理及结论】
I.测量氧气的体积采用的是排水法,将排出的水的用量筒收集起来,排出的水的体积就是氧气的体积;气体短管进长管出才能排出试剂瓶中的水,据此进行分析解答;
II.红砖粉末是否也可以作过氧化氢分解反应的催化剂的实验探究中,步骤a中他除了选用试管外,还用到上面列出的仪器有:水槽、橡胶塞和导管;步骤c的实验目的是:验证红砖粉末的化学性质是否改变;上述实验中缺少一个关键步骤是:实验前没有称量红砖粉末的质量.
解答 解:①控制氯酸钾的质量相等,才能比较出二氧化锰和氧化铜的催化效果,所以Ⅱ中x的数值为6.0g.故填:6.0;
【数据处理及结论】
I.测量氧气的体积采用的是排水法,将排出的水的用量筒收集起来,排出的水的体积就是氧气的体积;气体短管进长管出才能排出试剂瓶中的水,要将瓶内的水排出来,A和B都不可以,应该选择C装置作为实验装置;故填:C;
II.要将两支试管中的气体导出通入水中比较产生气泡的快慢,除了试管还要用到ghf三种仪器;催化剂是在化学反应里能改变其它物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质,从实验a中可看出红砖粉改变了过氧化氢分解的速度,实验b是用来检验红砖粉在反应前后的质量有没有发生变化,而该同学只称量了反应后红砖粉的质量,并没有称量反应前红砖粉的质量,实验c是用来证明红砖粉末在反应前后的化学性质没有改变.
故答案为:fgh;证明红砖粉末在反应前后的化学性质没有改变;实验开始没有称量红砖粉末的质量.
点评 本题难度不大,考查了影响化学反应速率的因素,掌握控制变量法的应用、量气装置等是正确解答本题的关键.

练习册系列答案
相关题目
4.下列各项为小明同学记录的物质燃烧现象,与事实不相符的是( )
| A. | 铁丝在氧气中燃烧时,生成四氧化三铁 | |
| B. | 木炭在氧气中燃烧时,发出白光 | |
| C. | 硫粉在氧气中燃烧时,产生明亮的蓝紫色火焰 | |
| D. | 镁条在空气中燃烧时,发出耀眼的白光 |
6.“鱼浮灵”主要成分是过碳酸钠(xNa2CO3•yH2O2),俗称固体双氧水、兴趣小组对其进行以下探究:
【性质探究】
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条复燃,说明有O2生成.
(2)取实验(1)中上层清液,测得溶液PH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有CO2(或二氧化碳)生成.
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质.
【工业制备】
(3)根据如表数据,你认为上述制备反应的最佳温度范围是15~20℃.
注:活性氧含量是指产品中能转化为O2的氧元素的质量分数.
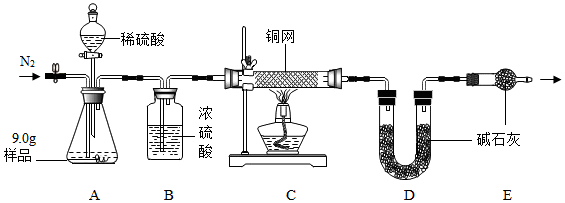
【组成测定】利用如图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成的测定(杂质对测定无影响)
查阅资料:①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品.②过碳酸钠能与酸反应放出CO2和O2.
(4)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2,其目的是将生成的O2、CO2送入装置C、D,使其被完全使残留在装置中的气体全部被吸收.
(5)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大(填“偏大”或“偏小”).
(6)实验测得C装置中铜网增重1.2g,D装置增重2.2g.该产品中活性氧含量为12%,属于合格品(填“一等品”“合格品”或“不合格品”);
【性质探究】
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条复燃,说明有O2生成.
(2)取实验(1)中上层清液,测得溶液PH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有CO2(或二氧化碳)生成.
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质.
【工业制备】
(3)根据如表数据,你认为上述制备反应的最佳温度范围是15~20℃.
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
【组成测定】利用如图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成的测定(杂质对测定无影响)
查阅资料:①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品.②过碳酸钠能与酸反应放出CO2和O2.
(4)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2,其目的是将生成的O2、CO2送入装置C、D,使其被完全使残留在装置中的气体全部被吸收.
(5)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大(填“偏大”或“偏小”).
(6)实验测得C装置中铜网增重1.2g,D装置增重2.2g.该产品中活性氧含量为12%,属于合格品(填“一等品”“合格品”或“不合格品”);

13.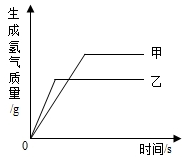 有甲、乙两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,则下列结论合理的是( )
有甲、乙两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,则下列结论合理的是( )
 有甲、乙两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,则下列结论合理的是( )
有甲、乙两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,则下列结论合理的是( )| A. | 金属活动性甲>乙 | B. | 生成氢气的质量甲>乙 | ||
| C. | 参与反应的硫酸质量甲<乙 | D. | 参与反应的金属质量甲<乙 |
11.下列物质属于混合物的是( )
| A. | 水蒸气 | B. | 二氧化碳气体 | C. | 洁净的空气 | D. | 冰水混合物 |
