题目内容
19. 金属是生产、生活中应用广泛的材料.
金属是生产、生活中应用广泛的材料.(1)酸菜等酸性的食物不宜用铁质器具长期盛放,因为铁会与酸反应而使铁质器具被腐蚀.
(2)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属.下列金属适宜船底镶嵌的是D(填选项).
A.Pb(铅) B.Cu C.Pt(铂) D.Zn
(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀.
①致密氧化膜能有效阻止铁锈蚀的原因是致密的氧化膜使铁与氧气(或空气)和水隔绝.
②“发蓝”过程的化学方程式如下,式中X的化学式为Fe3O4.
36Fe+4NaNO2+9NaNO3+26H2O=12X+13NaOH+13NH3↑
③为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质.由此可知该零件“发蓝”处理效果不好(填“好”或“不好”).
(4)甲同学设计了如图1实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
①B中反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,该反应的还原剂是CO.
②对该实验的分析正确的是AD.
A.实验结束时应先熄灭B处酒精灯
B.C中增加的质量与B中固体减少的质量相等
C.反应开始后通入2.8g一氧化碳可生成6.4g铜
D.反应结束后继续通入一氧化碳的目的是防止铜被氧化
③甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,理由是为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳.
(5)某学习小组欲测定铜的相对原子质量,设计如图2实验方案:
实验步骤:①连接好装置;②检查装置的气密性;③装入药品; ④打开分液漏斗活塞向锥形瓶中滴加入稀盐酸; ⑤一段时间后点燃酒精灯;⑥D中黑色固体完全变成红色,停止加热,待D中玻璃管冷却至室温,关闭分液漏斗活塞; ⑦数据处理.

请回答下列问题:
Ⅰ.补全实验步骤②.
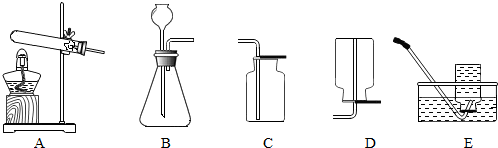
Ⅱ.若使制取氢气的装置随开随用,随关随停,下列装置可选用的是GH.

Ⅲ.B装置中水的作用是吸收盐酸挥发的氯化氢气体;长玻璃管的作用起安全作用,当B中气体压力过大时,水就会从玻璃管上端溢出;C装置的作用是干燥氢气.
Ⅳ.已知:CuO样品质量为m1克,E中增重为m2克,D中反应后固体质量为m3克,实际参加反应氢气的质量为m4克,试用m1,m2列出铜的相对原子质量的表达式$\frac{18{m}_{1}}{{m}_{2}}$-16.若无F装置,则对测定结果的影响偏小(填“偏大”、“偏小”、“无影响”),以下数据还能测定铜的相对原子质量的是ABC.
A.m2 m3B.m3 m4C.m1 m4 D.m2 m4
Ⅴ.请你评价实验有什么不妥之处,并说明原因实验中无法判断CuO是否完全反应,从而无法进行相应的计算.
分析 (1)根据铁会与酸反应生成进行分析;
(2)根据活泼性强的金属首先被腐蚀的变化规律,为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌的金属活动性应比铁的活动性强;
(3)①根据防锈就是使铁与水或氧气隔绝进行分析;
②根据质量守恒定律进行分析;
③根据铁能与硫酸铜反应生成硫酸亚铁和铜,可观察到铁丝表面出现红色固体,溶液由蓝色逐渐变为无色进行分析;
(4)①根据一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳进行分析;
②根据一氧化碳和氧化铜反应的注意事项以及物质质量的关系进行解答即可;
③根据装置A的作用进行分析;
(5)Ⅰ根据制取气体是先要检查装置的气密性进行分析;
Ⅱ要使装置随开随用,随关随停,那就要控制可以两种药品接触与分离;
Ⅲ水可以吸收盐酸挥发的氯化氢气体,同时与长玻璃管起到缓冲压力的作用,浓硫酸具有吸水性;
Ⅳ根据CuO样品的质量,E中增重水的质量分析铜的相对原子质量;F装置阻止空气中的水蒸气浸入E装置,结合方程式只要能包含铜或氧化铜的质量数据,列比例式就可求解;
Ⅴ根据实验中无法判断CuO是否完全反应.
解答 解:(1)铁的活动性在H的前面,能与酸反应,所以酸菜等酸性的食物不宜用铁质器具长期盛放;
(2)根据金属活动性顺序,五种金属的活动性强弱关系为锌>铁>铅>铜>铂,根据分析,为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌的金属是锌板,故选:D;
(3)①经“发蓝”处理后的钢铁零件表面上的蓝黑色氧化膜能够使铁与水或氧气隔绝,从而避免(减缓)钢铁腐蚀;
②根据质量守恒定律,反应前后原子的种类和数目不变,反应前:Fe原子数目为36,Na原子的数目为13,N原子的数目为13,O原子的数目为57,H原子的数目为52;反应后:Fe原子数目为0,Na原子的数目为13,N原子的数目为13,O原子的数目为13,H原子的数目为52;所以X的化学式为Fe3O4;
③如果氧化膜不致密,裸露出来的铁与硫酸铜的反应生成了铜和硫酸亚铁,反应的方程式为Fe+CuSO4 ═FeSO4 +Cu,所以将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质.由此可知该零件“发蓝”处理效果不好;
(4)①一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,该反应的还原剂是CO;
②A中的液体是排除二氧化碳气体;CO通入灼热的氧化铜,将其黑色氧化铜还原为红色的铜单质,并有二氧化碳气体生成,其反应方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;因为CO具有毒性,所以在D处将多余的CO点燃,防止污染空气;
A、实验结束时应先熄灭B处酒精灯,故A正确;
B、C中增加的质量是二氧化碳的质量,B中固体减小的质量是氧元素的质量,故质量不相等,故B错误;
C、该反应前后都要通入一氧化碳,所以反应开始后通入2.8g一氧化碳可生成6.4g铜,故C错误;
D、反应结束后继续通入一氧化碳的目的是防止铜被氧化,故D正确;
故选:AD;
③甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,理由是:为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳;
(5)Ⅰ、制取气体是先要检查装置的气密性;
ⅡF、装置当液体与固体接触时反应,由于另一端橡皮塞,关闭活塞不能使液体进入另一端使两种药品分离,所以不可选;
G、装置当液体与固体接触时反应,关闭活塞后液体在压力作用下进入长颈漏斗,使两种药品分离,反应停止,所以可选;
H、装置当把干燥管浸入液体,液体与固体接触时反应,把干燥管从液体中拿出,使两种药品分离,反应停止,所以可选;
故选:GH;
ⅢB是安全瓶,B中气体压力过大时,水就会从玻璃管上端溢出,D中所盛是水,水的作用吸收盐酸挥发的氯化氢气体,浓硫酸具有吸水性,干燥氢气;
Ⅳ设铜的相对原子质量为x
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
x+16 18
m1 m2
$\frac{x+16}{{m}_{1}}$=$\frac{18}{{m}_{2}}$
x=$\frac{18{m}_{1}}{m2}$-16;
F装置阻止空气中的水蒸气浸入E装置,若无F装置,E中增重m2变大,则对测定结果偏小;结合方程式只要能包含铜或氧化铜的质量数据,列比例式就可求解,故选ABC;
Ⅴ实验中无法判断CuO是否完全反应,从而无法进行相应的计算.
故答案为:(1)铁会与酸反应而使铁质器具被腐蚀;
(2)D;
(3)①致密的氧化膜使铁与氧气(或空气)和水隔绝;
②Fe3O4;
③不好;
(4)①CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,CO;
②AD;
③为了排尽装置中的空气,反应前已经通入一段时间的一氧化碳;
(5)Ⅰ.检查装置的气密性;
Ⅱ.GH;
Ⅲ.起安全作用,当B中气体压力过大时,水就会从玻璃管上端溢出;干燥氢气;
Ⅳ.$\frac{18{m}_{1}}{{m}_{2}}$-16,偏小,ABC;
Ⅴ.实验中无法判断CuO是否完全反应,从而无法进行相应的计算.
点评 本题考查了实验室制氢气的原理以及根据反应的原理选择合适的实验装置,学生的平常的化学学习中一定要注重对双基知识的学习,只有具备完整的知识系统,才能够很好的解决综合问题.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案| 符号名称 | 2个氧分子 | 七氧化二氯 | 2个钙离子 |
| 化学符号 | 2O2 | Cl2O7 | 2Ca2+ |



 有一研究性学习小组为测定某铜锌合金的成分,取l0g该合金经粉碎后放入烧杯中,再加入93.7g质量分数为20%的稀硫酸(反应后硫酸有剩余),反应过程中烧杯内固体物质的质量与反应时间的关系如图所示.请回答下列问题:
有一研究性学习小组为测定某铜锌合金的成分,取l0g该合金经粉碎后放入烧杯中,再加入93.7g质量分数为20%的稀硫酸(反应后硫酸有剩余),反应过程中烧杯内固体物质的质量与反应时间的关系如图所示.请回答下列问题: