题目内容
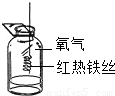
(1)CO在空气中燃烧的化学方程式为,将生成的气体通入已被石蕊溶液染成紫色的小花的集气瓶中,盖上玻璃片,出现的现象是;(2)集气瓶中的现象:铁丝在氧气中剧烈燃烧,,放出大量的热,有黑色固体生成.该反应的化学方程式为.
【答案】分析:根据一氧化碳和铁的性质,一氧化碳燃烧后生成二氧化碳,二氧化碳为酸性氧化物,溶于水所得溶液呈酸性;铁在氧气中能够剧烈燃烧,火星四溅,释放大量的热,最后生成黑色的四氧化三铁固体.
解答:解:(1)一氧化碳燃烧后生成二氧化碳,二氧化碳的水溶液呈酸性,可使紫色石蕊变红,故答案为:2CO+O2 2CO2;紫色的小花变红色
2CO2;紫色的小花变红色
(2)铁能与纯氧气剧烈反应,燃烧,火星四溅,释放大量的热,生成四氧化三铁黑色固体,故答案为:火星四溅;3Fe+2O2 Fe3O4
Fe3O4
点评:本题考查了一氧化碳的可燃性、二氧化碳水溶液的酸性、铁的燃烧现象,学生要对基础知识掌握牢固.
解答:解:(1)一氧化碳燃烧后生成二氧化碳,二氧化碳的水溶液呈酸性,可使紫色石蕊变红,故答案为:2CO+O2
 2CO2;紫色的小花变红色
2CO2;紫色的小花变红色(2)铁能与纯氧气剧烈反应,燃烧,火星四溅,释放大量的热,生成四氧化三铁黑色固体,故答案为:火星四溅;3Fe+2O2
 Fe3O4
Fe3O4点评:本题考查了一氧化碳的可燃性、二氧化碳水溶液的酸性、铁的燃烧现象,学生要对基础知识掌握牢固.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目