题目内容
5.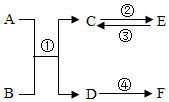 A~F都是初中化学中常见的物质,其中A、B、C是氧化物,且A是红棕色粉末,D、F均是单质.它们之间的转化关系如图所示(“→”表示物质转化的方向;部分反应物、生成物和反应条件未标出).
A~F都是初中化学中常见的物质,其中A、B、C是氧化物,且A是红棕色粉末,D、F均是单质.它们之间的转化关系如图所示(“→”表示物质转化的方向;部分反应物、生成物和反应条件未标出).(1)写出反应①的实验现象和化学方程式红棕色粉末变黑、Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)若F为紫红色物质,写出满足条件的反应④的化学方程式Fe+CuSO4=Cu+FeSO4.
分析 根据A~F都是初中化学中常见的物质,其中A、B、C是氧化物,且A是红棕色粉末,故A是氧化铁;A能与氧化物B反应生成单质的D和氧化物C,故B是一氧化碳,C是E二氧化碳,D是铁,紫红色固体F是铜,铁能与硫酸铜溶液反应生成铜;二氧化碳能与E相互转化,故E可能是碳酸钙,然后将推出的物质进行验证即可.
解答 解:A、B、C是氧化物,且A是红棕色粉末,故A是氧化铁;A能与氧化物B反应生成单质的D和氧化物C,故B是一氧化碳,C是E二氧化碳,D是铁,紫红色固体F是铜,铁能与硫酸铜溶液反应生成铜;二氧化碳能与E相互转化,故E可能是碳酸钙,带入框图,推断合理;
(1)氧化铁能与一氧化碳高温反应生成铁和二氧化碳,故会观察到红棕色粉末变黑,故填:红棕色粉末变黑;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)铁能与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4=Cu+FeSO4.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
13.下列物质的鉴别、除杂的试验中所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别CO和CO2 | 闻气味 |
| B | 鉴别稀硫酸和稀盐酸 | 加氯化钡溶液 |
| C | 除去生石灰中杂质石灰石 | 加水 |
| D | 除去氧化铜中碳粉 | 加稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
10.填写实验报告.
| 实验内容 | 实验现象 | 实验结论 |
| (1)用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻 | 蘸酒精的棉花燃烧. | 通过此实验,可以说明燃烧的条件之一是:燃烧需要可燃物. |
(2)从乒乓球和滤纸上各剪下一小片(同样大小),如图分别放在薄铜片的两侧,加热铜片的中部,观察现象.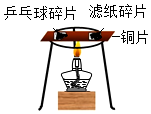 | 乒乓球碎片先燃烧. | 通过此实验,可以说明燃烧的条件之一是:温度需要可燃物的着火点. |
(3)点燃两支蜡烛,在其中一支蜡烛上倒扣一个A烧杯,另一支蜡烛放在B烧杯中.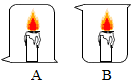 | A烧杯中蜡烛 熄灭,B烧杯中蜡烛正常燃烧. | 通过此实验,可以说明燃烧的条件之一是:可燃物要与氧气接触. |
17. 如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
 如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )| A. | t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A | |
| B. | 将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A | |
| C. | 升高温度可使接近饱和的C溶液变为饱和 | |
| D. | 当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A |
15.在含有稀H2SO4和CuSO4的混合溶液中,加入一定量的铁粉,充分反应后,发现有固体剩余,则下列叙述正确的是( )
| A. | 反应后溶液中一定有FeSO4 | B. | 反应后溶液中一定没有CuSO4 | ||
| C. | 剩余固体中一定不含铜 | D. | 剩余固体中一定没有铁 |