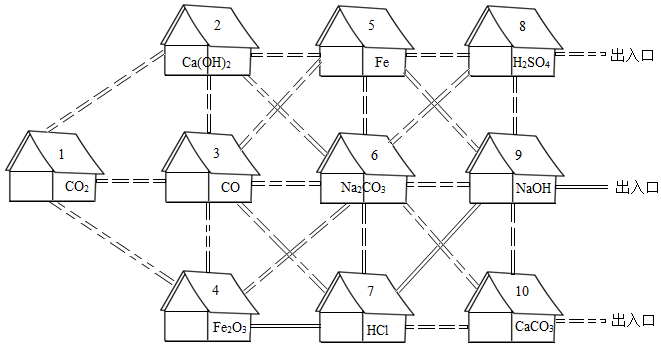
题目内容
6. 某化学研究小组对金属以及金属化合物的性质进行了研究.
某化学研究小组对金属以及金属化合物的性质进行了研究.(1)近期,“镉大米”危机席卷全国,各地纷纷抽检自查,结果令人震惊:全国有10%的大米镉超标.这里的镉是指D(填序号).
A.原子 B.离子 C.单质 D.元素
(2)摄入过量含镉等重金属盐会使人出现中毒症状,请你谈一下中毒的原因:镉等重金属离子能够破坏人体中的蛋白质.
(3)已知镉(Cd)在化合物中通常为+2价,镉在金属活动性顺序表中氢的前面,写出镉与盐酸反应的化学方程式该反应属于Cd+2HCl═CdCl2+H2↑,置换反应反应类型(化合,分解,复分解,置换之一)
(4)将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐滴加溶质质量分数10.4%的氯化钡溶液(杂质不与氯化钡溶液反应).实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示,试通过计算,求当滴加60g氯化钡溶液时生成的沉淀的质量.
分析 (1)全国有10%的大米镉超标,这里的镉是指元素;
(2)镉离子能够破坏人体中的蛋白质,从而能使人中毒;
(3)镉与盐酸反应生成氯化镉和氢气;
(4)硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)全国有10%的大米镉超标.这里的镉是指元素.
故选:D.
(2)摄入过量含镉等重金属盐会使人出现中毒症状,原因是镉等重金属离子能够破坏人体中的蛋白质.
故填:镉等重金属离子能够破坏人体中的蛋白质.
(3)镉与盐酸反应生成氯化镉和氢气,反应的化学方程式为:Cd+2HCl═CdCl2+H2↑,属于置换反应.
故填:Cd+2HCl═CdCl2+H2↑,置换反应.
(4)解:设生成沉淀的质量为x,
BaCl2+CuSO4═BaSO4↓+CuCl2,
208 233
40g×10.4% x
$\frac{208}{40g×10.4%}$=$\frac{233}{x}$,
x=4.66g,
答:当滴加60g氯化钡溶液时生成的沉淀的质量是4.66g.
点评 计算生成沉淀质量时,反应生成的沉淀消耗氯化钡溶液的质量是40g,而不是60g,要注意理解.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
16.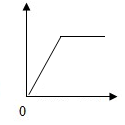 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )
 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 选项 | 横坐标 | 纵坐标 |
| A | 加热高锰酸钾制取氧气 | 氧元素的质量分数 |
| B | 向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量 | 产 生气体的质量 |
| C | 向一定量的澄清石灰水中加入碳酸钠溶液的质量 | 生成沉淀的质量 |
| D | 向一定量的铁粉中加入硫酸铜溶液 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
17.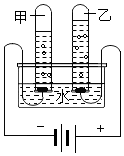 有关电解水的实验如图所示,下列叙述错误的是( )
有关电解水的实验如图所示,下列叙述错误的是( )
 有关电解水的实验如图所示,下列叙述错误的是( )
有关电解水的实验如图所示,下列叙述错误的是( )| A. | 水由氢气和氧气组成 | B. | 水由氢元素和氧元素组成 | ||
| C. | 试管甲中的气体是氢气 | D. | 试管乙中的气体是氧气 |
14.下列化学反应及反应类型与如图所示的微观变化对应的是( )


| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2化合反应 | |
| B. | 2HI+Cl2═2HCl+I2 置换反应 | |
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ 分解反应 | |
| D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
1.根据如图提供的信息进行判断,下列对相应微粒的描述中,不正确的是( )
| A. | 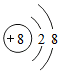 带负电荷 | B. | 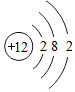 易形成阳离子 | C. | 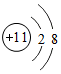 化学性质活泼 | D. | 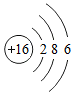 非金属元素原子 |
11.近年来有人提出了利用处理后的海水(主要成分是氯化钠溶液)吸收含二氧化硫的废气,该方法的流程如图所示.
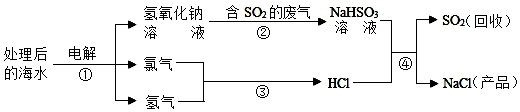
下列说法正确的是( )

下列说法正确的是( )
| A. | 图中反应①属于分解反应,反应④属于复分解反应 | |
| B. | 反应中硫元素的化合价发生变化 | |
| C. | 反应③中,反应前后分子数目没有变化 | |
| D. | 将5gSO2溶于95g水形成溶液,其溶液的溶质质量分数为5% |
18.下列说法正确的是( )
| A. | 钾肥不但能促进农作物枝叶茂盛,叶色浓绿,还能提高产量 | |
| B. | 缺少维生素A会导致坏血病 | |
| C. | 羊毛、塑料、橡胶等都是重要的有机合成材料 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
15.科学家最近发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的围观示意图,下列说法错误的是( )
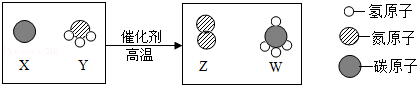

| A. | X、Y、Z、W四种物质中有三种物质是由分子构成的 | |
| B. | W物质中碳元素的质量分数为75% | |
| C. | 参加反应的X、Y两物质的粒子个数比为1:1 | |
| D. | 该反应属于置换反应 |