题目内容
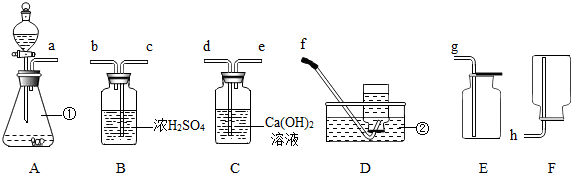
17.通过一年的化学学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置,根据如图回答下列问题:
(1)关闭A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则A装置是否漏气?不漏气(填“漏气”、“不漏气”或“无法确定”),若用A、D装置制取氧气,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)在用A装置制取二氧化碳时,只能用D装置收集二氧化碳的原因是二氧化碳的密度比空气大、能溶于水.
(3)若用B、E装置制取氧气,当实验结束时,甲同学先熄灭了酒精灯,忘记将导管从水中取出,在水未进入导管之前,可采取的补救措施有:重新加热至导管口有气泡冒出,再移出导管(合理均可)(写一条)
(4)氨气(NH3)是一种密度比空气小且极易溶于水的气体,对空气有污染,其水溶液称为氨水.当你选用加热氯化铵和氢氧化钙的固体混合物来制取氨气时,你认为制取氨气最好选择的发生和收集装置是BF(填字母代号).
分析 (1)从图中可以看出在密闭的容器中,液面没有下降,可以根据压强来判断;A装置属于固液常温型,过氧化氢制取氧气可用此装置,据反应原理书写方程式;
(2)二氧化碳密度比空气大且能溶于水,所以只能用向上排空气法收集;
(3)先熄灭了酒精灯,忘记将导管从水中取出,在水未进入导管之前,可采取的补救措施有:可采取的补救措施有:①重新加热至导管口有气泡冒出,再移出导管;从试管口拔掉带导管的胶塞;
(4)用加热氯化铵和氢氧化钙的固体混合物来制取氨气时,属于固体加热型,故选发生装置B,氨气是一种密度比空气小且极易溶于水的气体,宜采取向下排气法收集,为防止氨气扩散可利用水吸收氨气.
解答 解:(1)若装置漏气,装置内的气体向外逸出,装置内的气体压强减小,在外界大气压的作用下长颈漏斗内的液面将会下降,而现在装置内的液面没有下降,说明装置不漏气;
A装置属于固液常温型,过氧化氢制取氧气可用此装置,反应方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)二氧化碳密度比空气大且能溶于水,所以只能用向上排空气法收集;
(3)先熄灭了酒精灯,忘记将导管从水中取出,在水未进入导管之前,可采取的补救措施有:可采取的补救措施有:①重新加热至导管口有气泡冒出,再移出导管;从试管口拔掉带导管的胶塞;
(4)用加热氯化铵和氢氧化钙的固体混合物来制取氨气时,属于固体加热型,故选发生装置B,氨气有刺激性气味,扩散到空气中会造成空气污染,收集时应防止氨气扩散到空气中;为防止氨气扩散到空气中,可利用“极易溶于水的气体”这一性质用水吸收多余的氨气;
故答案为:(1)不漏气;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)二氧化碳的密度比空气大、能溶于水;
(3)重新加热至导管口有气泡冒出,再移出导管(合理均可);
(4)BF.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了气密性检查、注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案| A. | K+、Cu2+、SO42- | B. | Ba2+、K+、Cl- | C. | NH4+、SO42-、Cl- | D. | Na+、Fe3+、NO3 |
| A. | 石蜡燃烧 加热食盐水有晶体析出 | |
| B. | 动植物呼吸 铝片放在空气中变暗 | |
| C. | 冬天窗户上出现冰花 铁制小刀在潮湿的空气中生锈 | |
| D. | 灯泡通电发光 汽油挥发 |
| A. | 天然气燃烧 | B. | 面包发霉 | C. | 灯泡发光 | D. | 久置的牛奶变酸 |
①2H ②2NH3 ③SO2 ④${\;}_{Cu}^{-2}$O ⑤Mg2+.
| A. | 表示原子个数的是② | B. | 表示离子所带电荷数的是④ | ||
| C. | 表示分子中原子个数的是③ | D. | 表示分子个数的是① |