题目内容
11.在硝酸铜、硝酸锌、硝酸亚铁混合溶液中加入铝粉,充分反应后过滤.(1)若滤纸上有两种金属,则这两种金属是Cu、Fe(填化学式)
(2)若滤液中只有一种溶质,则这种溶质是Al(NO3)3(填化学式)
分析 铝比锌活泼,锌比铁活泼,铁比铜活泼.
解答 解:(1)在硝酸铜、硝酸锌、硝酸亚铁混合溶液中加入铝粉,铝先和硝酸铜反应,当硝酸铜完全反应后,如果铝有剩余,再和硝酸亚铁反应,以此类推,最后和硝酸锌反应,若滤纸上有两种金属,则这两种金属是Cu、Fe;
(2)由以上分析可知,若滤液中只有一种溶质,则这种溶质是Al(NO3)3,即硝酸铜、硝酸锌和硝酸亚铁都完全反应.
故填:Cu、Fe;Al(NO3)3.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.稀释浓硫酸时,一定要( )
| A. | 把浓硫酸沿着器壁慢慢的注入水中 | |
| B. | 把水沿着器壁慢慢地倒入浓硫酸中 | |
| C. | 把水迅速地倒入浓硫酸中 | |
| D. | 将浓硫酸和水按一定比例同时倒入量筒中 |
2.PM2.5是指2.5微米以下的细微颗粒物,它对人体健康和环境质量的影响很大.下列措施对PM2.5的治理起不到积极作用的是( )
| A. | 城市道路定时洒水 | B. | 大力植树造林 | ||
| C. | 焚烧垃圾 | D. | 加强建筑工地扬尘控制 |
19.氯气(Cl2)是黄绿色气体,溶于水时部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O═HCl+HClO.产物中,次氯酸(HClO)是一种弱酸.氯气溶于水所得溶液称为氯水,它具有很强的漂白性.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.晓红同学对“氯水使品红试纸褪色”产生浓厚兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】猜想1:氯水中的水使品红试纸褪色; 猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色; 猜想4:氯水中的HClO使品红试纸褪色.
【实验探究】
【结论】学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是石蕊试液变红色,后红色溶液变成无色.
【拓展】铁能在氯气中燃烧生成氯化铁,请写出该反应的化学方程式2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】猜想1:氯水中的水使品红试纸褪色; 猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色; 猜想4:氯水中的HClO使品红试纸褪色.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| ①把品红试纸放入水中 | 品红试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放入氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③把品红试纸放入稀盐酸中 | 试纸不褪色 | 猜想3不成立 |
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是石蕊试液变红色,后红色溶液变成无色.
【拓展】铁能在氯气中燃烧生成氯化铁,请写出该反应的化学方程式2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
1.实验室制取CO2的有关操作如图,不正确的是( )
| A. | 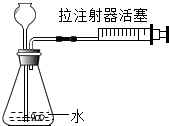 检查气密性 | B. | 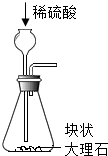 制气 | ||
| C. | 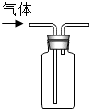 收集 | D. |  验满 |