题目内容
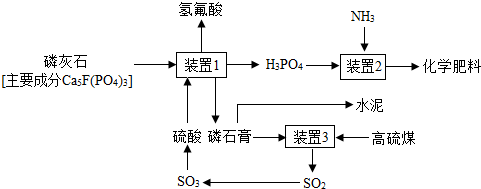
19.利用图甲装置探究“MnO2的用量对H2O2分解反应的影响”,实验中H2O2的溶质质量分数为3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比.反应放热忽略不计.)(1)MnO2在此反应中起催化作用.
(2)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出H2O2的用量越多,产生的氧气越多.
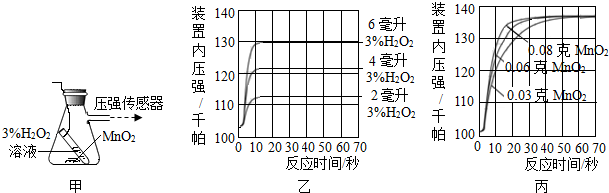
(3)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线.曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图C(选填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求.

分析 (1)过氧化氢在二氧化锰的催化作用下生成水和氧气;
(2)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(3)根据图中给出的比例分析.
解答 解:过氧化氢在二氧化锰的催化作用下生成水和氧气,其中二氧化锰起到催化作用;
(2)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(3)由图示可知3%H2O2溶液8毫升与0.08克MnO2混合,分解速度达到实验要求,若MnO2的质量有4克需要3%H2O2溶液为$\frac{4g}{0.08g}$×8mL=400mL.
故答案为:(1)催化;
(2)H2O2的用量越多,产生的氧气越多;
(3)C.
点评 本题通过对比实验结果的分析,找到事物的内在联系,考查了学生分析问题的能力,同时也是对影响反应速率因素这一知识点的重点考查.

练习册系列答案
相关题目
14.为测定某种铝铜合金的质量分数,探究小组进行了如表实验:
(1)所用稀硫酸溶质的质量分数为多少?
(2)该铝铜合金中铝的质量分数是多少?
| 实验端号 | 铝铜合金的质量(g) | 加入稀硫酸的质量 | 生成H2的质量(g) |
| 实验1 | 30 | 392 | 2 |
| 实验2 | 30 | 588 | 3 |
| 实验3 | 30 | 600 | 2 |
(2)该铝铜合金中铝的质量分数是多少?
 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶解于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,现象如图所示(ABC表示沉淀变化,OBC表示气体变化).
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶解于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,现象如图所示(ABC表示沉淀变化,OBC表示气体变化).