题目内容
18. 如图,A、B、C、D、E、F分别表示六种物质,A是目前世界年产量最高的金属,B物质溶于水后其溶液为蓝色,C是地壳中含量最高的金属元素组成的单质,D和E两种物质中不含相同种类的元素,E会造成温室效应,“
如图,A、B、C、D、E、F分别表示六种物质,A是目前世界年产量最高的金属,B物质溶于水后其溶液为蓝色,C是地壳中含量最高的金属元素组成的单质,D和E两种物质中不含相同种类的元素,E会造成温室效应,“ ”或“
”或“ ”表示两种物质之间能发生反应,“
”表示两种物质之间能发生反应,“ ”表示一种物质可以转化为另一种物质,部分反应物和生成物已略去,请回答下列问题:
”表示一种物质可以转化为另一种物质,部分反应物和生成物已略去,请回答下列问题:(1)请写出D、E、F的化学式:DHCl ECO2 FCaCO3;
(2)写出B与C反应的化学方程式:2Al+3CuSO4═Al2(SO4)3+3Cu;
(3)写出D与足量C反应的现象:银白色固体逐渐减少,表面有气泡产生,放热.
分析 根据“A是目前世界年产量最高的金属”,则推测A为铁;根据“B物质溶于水后其溶液为蓝色”,则推测B物质中含有铜元素;根据“C是地壳中含量最高的金属元素组成的单质”,则推测C为铝;根据“E会造成温室效应”,则推测E为二氧化碳;结合图框,推测:D可能为稀盐酸,F可能为碳酸钙,代入检验.
解答 解:
根据“A是目前世界年产量最高的金属”,则推测A为铁;根据“B物质溶于水后其溶液为蓝色”,则推测B物质中含有铜元素;根据“C是地壳中含量最高的金属元素组成的单质”,则推测C为铝;根据“E会造成温室效应”,则推测E为二氧化碳;结合图框,推测:D可能为稀盐酸,F可能为碳酸钙,代入检验,符合题意.则:
(1)根据分析,D可能为稀盐酸,E为二氧化碳,F可能为碳酸钙,则D、E、F的化学式分别为:HCl、CO2、CaCO3;
(2)根据分析,B与C反应,可能为铝与硫酸铜溶液的反应,故其反应的化学方程式:2Al+3CuSO4═Al2(SO4)3+3Cu;
(3)根据分析,D与足量C反应,即铝与稀盐酸反应,其反应的现象:银白色固体逐渐减少,表面有气泡产生,放热.
故答案为:
(1)HCl、CO2、CaCO3;(2)2Al+3CuSO4═Al2(SO4)3+3Cu;(3)银白色固体逐渐减少,表面有气泡产生,放热.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.(1)用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.(结果精确到0.1)
(2)某化学小组在实验室用CO和Fe2O3在密闭容器中隔绝空气加强热模拟炼铁过程,一段时间后收集到如表数据:
①预期看到的实验现象应该是红色固体变成黑色固体;
②实验过程中看到的实验现象与预期的现象相符.但查阅资料可知:CO还原Fe2O3时在一定条件下可生成铁的其它氧化物FeO和Fe3O4,二者也均为黑色固体,发生的化学反应方程式分别为Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2FeO+CO2、3Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2.
③表中b的值为4.4;物质M的化学式为FeO.
(2)某化学小组在实验室用CO和Fe2O3在密闭容器中隔绝空气加强热模拟炼铁过程,一段时间后收集到如表数据:
| 物质 | CO | Fe2O3 | Fe | M | CO2 |
| 反应前质量(g) | 2.8 | 16 | 0 | 0 | 0 |
| 反应后质量(g) | 0 | 0 | 0 | a | b |
②实验过程中看到的实验现象与预期的现象相符.但查阅资料可知:CO还原Fe2O3时在一定条件下可生成铁的其它氧化物FeO和Fe3O4,二者也均为黑色固体,发生的化学反应方程式分别为Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2FeO+CO2、3Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2.
③表中b的值为4.4;物质M的化学式为FeO.
9.将一定量的铁粉加入AgNO3、Cu(NO3)2和Zn(NO3)2的混合溶液中,充分反应后过滤,向滤液中加入稀盐酸,有白色沉淀产生.下列结论正确的是( )
| A. | 滤渣中只含有Ag | B. | 滤渣中可能有Ag、Cu、Fe | ||
| C. | 滤液中可能含有AgNO3、Cu(NO3)2 | D. | 滤液中只含有Fe(NO3)2、Zn(NO3)2 |
6.下列图示的实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
13.下列有关二氧化碳的用途中,不正确的是( )
| A. | 作气体肥料 | B. | 作化工产品的原料 | ||
| C. | 用于灭火 | D. | 供给呼吸 |
3.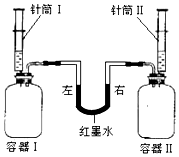 按如图进行实验,同时将针筒内全部液体迅速注入容器中,实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
按如图进行实验,同时将针筒内全部液体迅速注入容器中,实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
(1)实验a中,容器Ⅰ内产生的现象是澄清石灰水变浑浊,针筒Ⅱ中水的体积V=10 mL.红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内硫酸足量且溶质质量分数相同,产生气泡较剧烈的是容器Ⅰ (填“Ⅰ”或“Ⅱ”),红墨水液面位置的变化情况是B(填字母编号).
A.开始左高右低,最终左低右高
B.开始左低右高,最终左高右低
出现该变化的原因:开始时锌和稀硫酸的反应速率比铁和稀硫酸的反应速率快,单位时间内产生的氢气多;最终铁和稀硫酸反应生成的氢气比锌和稀硫酸反应生成的氢气多.
 按如图进行实验,同时将针筒内全部液体迅速注入容器中,实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
按如图进行实验,同时将针筒内全部液体迅速注入容器中,实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.| 实验编号 | 容器Ⅰ | 针筒Ⅰ | 容器Ⅱ | 针筒Ⅱ | 红墨水液面位置 |
| a | 二氧化碳 (充满) | 10mL澄清石灰水 | 二氧化碳 (充满) | V mL水 | 保持左高右低 |
| b | 0.5g锌粉 | 15mL20%的稀硫酸 | 0.5g铁粉 | 15mL20%的稀硫酸 |
(2)实验b中,针筒Ⅰ、Ⅱ内硫酸足量且溶质质量分数相同,产生气泡较剧烈的是容器Ⅰ (填“Ⅰ”或“Ⅱ”),红墨水液面位置的变化情况是B(填字母编号).
A.开始左高右低,最终左低右高
B.开始左低右高,最终左高右低
出现该变化的原因:开始时锌和稀硫酸的反应速率比铁和稀硫酸的反应速率快,单位时间内产生的氢气多;最终铁和稀硫酸反应生成的氢气比锌和稀硫酸反应生成的氢气多.
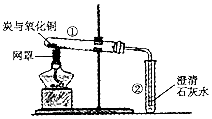 用木炭还原氧化铜的实验如图
用木炭还原氧化铜的实验如图 如图是炼铁高炉模拟图,其中产生铁的化学方程式(赤铁矿石的主要成分为氧化铁)为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,金属资源是不可再生资源,请列举一条保护金属资源的途径回收废旧金属.
如图是炼铁高炉模拟图,其中产生铁的化学方程式(赤铁矿石的主要成分为氧化铁)为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,金属资源是不可再生资源,请列举一条保护金属资源的途径回收废旧金属.