题目内容
14.如图是实验室制取气体的一些装置,据图回答有关问题.
(1)写出指定仪器的名称:①试管;②集气瓶.
(2)实验室中用加热氯酸钾和二氧化锰的混合物制取并收集氧气,可选用CD或CE(填装置序号),该反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)若用G图的装置测量生成CO2气体的体积,需在集气瓶内的水面上放一层植物油,其目的是防止二氧化碳和水反应.
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须控制反应速度否则引起装置炸裂.你认为A~F中最适合制取乙炔气体的发生装置是A;如果用H装置收集乙炔,气体应从a(填“a”或“b”)端管口通入.
(5)如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.(已知铜和氧气在加热的条件下反应生成氧化铜)

①根据下表提供的实验数据,完成下表
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 9mL | 15% |
③若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因是铜粉的量不足;未待装置完全冷却至室温就读数.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;
(3)根据二氧化碳易溶于水,二氧化碳会与水反应生成碳酸进行分析;
(4)根据实验室制取乙炔的反应物是固体和液体,反应条件是常温,该反应必须控制反应速度否则引起装置炸裂,乙炔密度比水小,难溶于水进行分析;
(5)①根据注射器内气体减少的量就是氧气的量进行分析;
②从两种装置的区别进行分析;
③根据测定空气中氧气的体积分数实验的原理、注意事项分析回答.
解答 解:(1)通过分析题中所指仪器的作用可知,①是试管,②是集气瓶;
(2)实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,所以制取并收集氧气,可选用CD或CE,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)二氧化碳易溶于水,二氧化碳会与水反应生成碳酸,所以用G图的装置测量生成CO2气体的体积,需在集气瓶内的水面上放一层植物油,其目的是防止二氧化碳和水反应;
(4)实验室制取乙炔的反应物是固体和液体,反应条件是常温,该反应必须控制反应速度否则引起装置炸裂,乙炔密度比水小,难溶于水,所以最适合制取乙炔气体的发生装置是A,用H装置收集乙炔,气体应从a端管口通入;
(5)①注射器内气体减少的量就是氧气的体积,则实验测得空气中氧气的体积分数为:$\frac{15mL-9mL}{25mL+15mL}$×100%=15%;
②装置二与装置一装置比较,装置二中的气球在玻璃管的后部,更易让空气流通,氧气与铜能充分反应;
③在测定空气中氧气的体积分数时,实验后发现测定氧气的体积分数低于五分之一,可能的原因有:①铜粉的量可能不足,没有将氧气消耗尽;②装置可能漏气;③实验中可能未冷却至室温就读数等.
故答案为:(1)试管,集气瓶;
(2)CD或CE,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)防止二氧化碳和水反应;
(4)A,a;
(5)①15%;
②装置二中,能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应;
③铜粉的量可能不足,没有将氧气消耗尽;实验中可能未冷却至室温就读数等.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 走进文言文系列答案
走进文言文系列答案| A. | 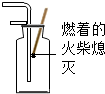 二氧化碳的验满 | B. | 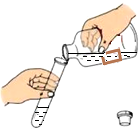 倾倒液体 | C. | 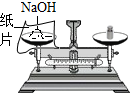 称量氢氧化钠 | D. | 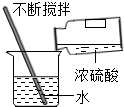 稀释浓硫酸 |
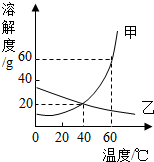 如图是甲、乙两种固体的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体的溶解度曲线,下列叙述正确的是( )| A. | 20℃时,甲的溶解度大于乙的溶解度 | |
| B. | 40℃时,甲、乙溶液中溶质的质量分数相等 | |
| C. | 采用降温的方法可将乙的不饱和溶液转化为饱和溶液 | |
| D. | 60℃时,甲的饱和溶液中溶质与溶液的质量比为3:8 |
 如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )
如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )| A. | 该元素是金属元素 | B. | 该元素的原子序数为7 | ||
| C. | 该元素的相对原子质量是14.01 | D. | 氮的元素符号为N2 |
| A. | 氯化亚铁溶液是浅绿色的 | |
| B. | 汽油洗油污是利用了乳化原理 | |
| C. | 升高温度既能加快溶解速率又能增大溶解度 | |
| D. | 溶液中溶质只有一种 |

 今年全国两会,“创客”首次“闯入”《政府工作报告》.在创新、创造的过程中也离不开化学的贡献. 请回答下列问题:
今年全国两会,“创客”首次“闯入”《政府工作报告》.在创新、创造的过程中也离不开化学的贡献. 请回答下列问题: