题目内容
11.实验室用6.5克锌与100克稀盐酸恰好完全反应,可制得氢气的质量是多少?反应后所得溶液的溶质质量分数是多少?(计算结果保留一位小数)分析 锌和稀盐酸反应生成氯化锌和氢气,根据锌的质量和反应的化学方程式可以计算氢气的质量和生成氯化锌的质量,进一步可以计算反应后所得溶液的溶质质量分数.
解答 解:设生成氯化锌质量为x,生成氢气质量为y,
Zn+2HCl═ZnCl2+H2↑,
65 136 2
6.5g x y
$\frac{65}{6.5g}$=$\frac{136}{x}$=$\frac{2}{y}$,
x=13.6g,y=0.2g,
反应后所得溶液的溶质质量分数是:$\frac{13.6g}{6.5g+100g-0.2g}$×100%=12.8%,
答:可制得氢气的质量是0.2g,反应后所得溶液的溶质质量分数是12.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.根据日本共同社2011年3月15日中午十一点的消息,福岛第一核电站四号机组发生了氢气爆炸,下列属于氢气化学性质的是( )
| A. | 密度小 | B. | 无色、无味的气体 | ||
| C. | 氢气不纯燃烧可能发生爆炸 | D. | 分子小,运动快,散热效果好 |
16.正确的化学实验操作对实验结果、人身安全非常重要.下图中的实验操作正确的是( )
| A. | 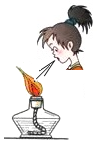 熄灭酒精灯 | B. |  倾倒液体 | C. | 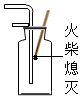 气体验满 | D. |  液体过滤 |
3.用硬水洗衣服,既浪费肥皂,还洗不干净,生活中要使硬水软化,可采用的方法是( )
| A. | 过滤 | B. | 搅拌 | C. | 沉淀 | D. | 煮沸 |
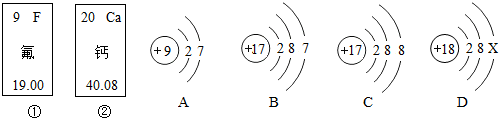
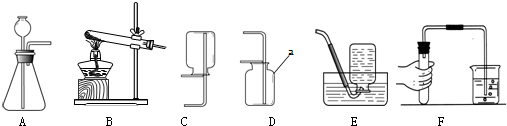
 如图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题.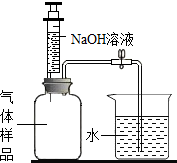 在我国北方地区,由于冬季天气寒冷,一般农村家庭都有地下菜窖,以储存冬季的蔬菜等食物.但常有人员进入菜窖时因CO2含量过高而导致死亡的报道.在北方某地区的九年级兴趣小组同学看了报道后,决定对菜窖内CO2的含量进行探究.
在我国北方地区,由于冬季天气寒冷,一般农村家庭都有地下菜窖,以储存冬季的蔬菜等食物.但常有人员进入菜窖时因CO2含量过高而导致死亡的报道.在北方某地区的九年级兴趣小组同学看了报道后,决定对菜窖内CO2的含量进行探究.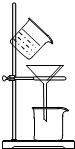 (1)写出过滤操作中所用到的玻璃仪器的名称:烧杯、漏斗、玻璃棒;
(1)写出过滤操作中所用到的玻璃仪器的名称:烧杯、漏斗、玻璃棒;