题目内容
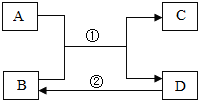 A、B、C、D是初中化学常见物质,它们之间有如下反应及转化关系(反应条件未标出).
A、B、C、D是初中化学常见物质,它们之间有如下反应及转化关系(反应条件未标出).(1)若①、②都是置换反应,C是红色固体,则反应①的化学方程式为
(2)若①不是置换反应,B、D组成元素种类相同,则反应①的化学方程式为
(3)若B、D都属于盐,其中D难溶于水,则反应①的化学方程式为
考点:物质的鉴别、推断,置换反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:(1)根据A、B、C、D是初中化学常见物质,①、②都是置换反应,C是红色固体,常见的红色固体有:红磷、氧化铁、铜,所以C是铜,猜想A是硫酸铜,B是铁,D就是硫酸亚铁,然后将推出的物质代入转化关系中验证即可;
(2)根据A、B、C、D是初中化学常见物质,①不是置换反应,B、D组成元素种类相同,猜想B是一氧化碳,D是二氧化碳,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,二氧化碳和木炭高温会生成一氧化碳,然后将推出的各种物质代入转化关系中验证即可;
(3)根据A、B、C、D是初中化学常见物质,B、D都属于盐,其中D难溶于水,猜想B是碳酸钠,A是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,然后将推出的各种物质代入转化关系中验证即可.
(2)根据A、B、C、D是初中化学常见物质,①不是置换反应,B、D组成元素种类相同,猜想B是一氧化碳,D是二氧化碳,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,二氧化碳和木炭高温会生成一氧化碳,然后将推出的各种物质代入转化关系中验证即可;
(3)根据A、B、C、D是初中化学常见物质,B、D都属于盐,其中D难溶于水,猜想B是碳酸钠,A是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,然后将推出的各种物质代入转化关系中验证即可.
解答:解:(1)A、B、C、D是初中化学常见物质,①、②都是置换反应,C是红色固体,常见的红色固体有:红磷、氧化铁、铜,所以C是铜,猜想A是硫酸铜,B是铁,D就是硫酸亚铁,铁和硫酸铜反应生成硫酸亚铁和铜,硫酸亚铁和锌反应生成硫酸锌和铁,推出的物质均满足题中的转化关系,所以反应①的化学方程式为:Fe+CuSO4=FeSO4+Cu;
(2)A、B、C、D是初中化学常见物质,①不是置换反应,B、D组成元素种类相同,猜想B是一氧化碳,D是二氧化碳,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,二氧化碳和木炭高温会生成一氧化碳,二氧化碳和一氧化碳的组成元素相同,所以反应①的化学方程式为:CuO+CO
Cu+CO2;
(3)A、B、C、D是初中化学常见物质,B、D都属于盐,其中D难溶于水,猜想B是碳酸钠,A是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,氯化钙、碳酸钙都属于盐,推出的物质均满足题中的转化关系,所以反应①的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.
故答案为:(1)Fe+CuSO4=FeSO4+Cu;
(2)CuO+CO
Cu+CO2;
(3)Na2CO3+CaCl2=CaCO3↓+2NaCl.
(2)A、B、C、D是初中化学常见物质,①不是置换反应,B、D组成元素种类相同,猜想B是一氧化碳,D是二氧化碳,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,二氧化碳和木炭高温会生成一氧化碳,二氧化碳和一氧化碳的组成元素相同,所以反应①的化学方程式为:CuO+CO
| ||
(3)A、B、C、D是初中化学常见物质,B、D都属于盐,其中D难溶于水,猜想B是碳酸钠,A是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,氯化钙、碳酸钙都属于盐,推出的物质均满足题中的转化关系,所以反应①的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.
故答案为:(1)Fe+CuSO4=FeSO4+Cu;
(2)CuO+CO
| ||
(3)Na2CO3+CaCl2=CaCO3↓+2NaCl.
点评:在解此类题时,首先分析题中各物质的反应关系,然后结合学过的知识和反应进行有目的猜想,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
如图所示的微观变化与下列反应及反应类型能对应起来的是( )
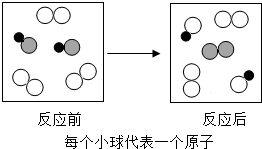

| A、2NO+O2=2NO2 化合反应 |
| B、2H2S+O2=2H2O+2S↓ 置换反应 |
| C、2HI=H2+I2 分解反应 |
| D、2HI+Cl2=2HCl+I2 置换反应 |
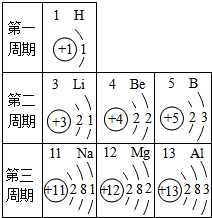 根据如图提供的信息,下列判断正确的是( )
根据如图提供的信息,下列判断正确的是( )| A、元素所在的周期数等于其原子的最外层电子数 |
| B、钠离子核外有三个电子层 |
| C、第二、三周期元素的原子从左至右最外层电子数逐渐增多 |
| D、在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg2- |
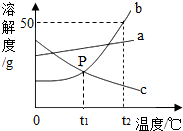 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
 现有H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计如下实验方案:取四份混合溶液各100g,分别缓慢加入到50g、100g、150g、200g某NaOH溶液中,测得四组实验数据如表:
现有H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计如下实验方案:取四份混合溶液各100g,分别缓慢加入到50g、100g、150g、200g某NaOH溶液中,测得四组实验数据如表: