题目内容
(8分)某化工厂排放的废水中只含有盐酸和MgCl2两种物质。小明同学向采集来的62.8 g废水样品中,慢慢加入20%的NaOH溶液至恰好完全反应时,消耗NaOH溶液60g。将生成的沉淀物过滤出,经水洗、干燥后称重为5.8g。
求:废水中盐酸的质量分数
6.0%
【解析】
试题分析:根据沉淀的质量计算出与氯化镁反应消耗氢氧化钠的质量,再计算出与盐酸反应的氢氧化钠质量;根据氢氧化钠与稀盐酸反应的化学方程式进行计算即可。具体步骤如下:
【解析】
设:与MgCl2反应的NaOH的质量为x
MgCl2+2NaOH===Mg(OH) 2 ↓+2NaCl
80 58
X 5.8g
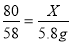 x=8g
x=8g
与盐酸反应的氢氧化钠的质量为:60g×20%-8g=4g
设:溶液中HCl的质量为y
HCl + NaOH===NaCl+H2O
36.5 40
Y 4g
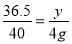 y=3.65g
y=3.65g
盐酸的质量分数为:
考点:溶质质量分数与化学方程式相结合的计算题。

 名校课堂系列答案
名校课堂系列答案(6分)化学与生活、生产和科研密切相关。
(1)实验室要把50g 98%的浓硫酸稀释成20%的硫酸溶液,需加水的质量为 g。
(2)“钙强化营养盐”的配料表:氯化钠、活性钙、碘酸钾。该盐中的营养成分表如下:
项目 | 能量 | 蛋白质 | 脂肪 | 糖类 | 钠 | 钙 | 碘 |
每100克 | 0 kJ | 0 g | 0 g | 0 g | 35385mg | 250 mg | 2 mg |
食用这种盐对人体健康有利的是___________(填序号)。
A.防止引起贫血病
B.维持人体内的水分和维持体液恒定的pH
C.防止甲状腺肿大
D.有助于骨骼和牙齿更坚固
(3)下列物品中,由有机合成材料制成的是 。
a.合成橡胶手套 b.塑料保鲜膜 c.棉布围裙 d.不锈钢炊具