题目内容
11. 将等质量的锌粉和铁粉分别放入质量相等、浓度相同的稀盐酸中,生成氢气的质量(m)随时间(t)的变化曲线如图.对于该图象的理解,下列说法正确的有( )
将等质量的锌粉和铁粉分别放入质量相等、浓度相同的稀盐酸中,生成氢气的质量(m)随时间(t)的变化曲线如图.对于该图象的理解,下列说法正确的有( )①反应结束后稀盐酸都无剩余
②反应结束后两种金属一定都有剩余
③反应后得到两种溶液的质量不相等
④反应结束后消耗两种金属的质量相等
⑤A的反应速率比B快
⑥A的金属活动性比B强.
| A. | ①②③ | B. | ④①⑥ | C. | ①③⑤⑥ | D. | ①③⑥ |
分析 锌和稀盐酸反应生成氯化锌和氢气,铁和稀盐酸反应生成氯化亚铁和氢气;
生成的氢气来自于稀盐酸中,根据图中提供的信息可以判断相关方面的问题.
解答 解:①如果稀盐酸过量,则生成的氢气质量不相等,如果铁恰好和稀盐酸反应,则锌不足,生成的氢气质量小于铁和稀盐酸反应生成氢气的质量,如果锌恰好和稀盐酸反应,则铁过量,和铁反应的稀盐酸不足,因此反应结束后稀盐酸都无剩余,该选项说法正确;
②反应结束后,如果锌恰好和稀盐酸反应,则铁过量,和铁反应的稀盐酸不足,因此两种金属不一定都有剩余,该选项说法不正确;
③反应结束后稀盐酸都无剩余,则生成氯化锌的质量大于氯化亚铁的质量,又因为生成氢气的质量相等,因此反应后得到两种溶液的质量不相等,该选项说法正确;
④因为反应的稀盐酸质量相等,因此反应结束后消耗两种金属的质量不相等,消耗锌的质量大,该选项说法不正确;
⑤由图中可知,A和稀盐酸反应需要的时间比B短,说明A的反应速率比B快,该选项说法正确;
⑥由图中可知,A和稀盐酸反应需要的时间比B短,说明A的金属活动性比B强,该选项说法正确.
故选:C.
点评 本题结合图象对金属与酸的反应进行了细致的考查,能很好的考查学生对知识的掌握和应用能力,要结合相关知识认真分析.

练习册系列答案
相关题目
2.党的十八大报告中把“生态文明建设”首次提升到更高的战略层面,要求加大自然生态系统和环境保护力度.近年来,我国多地出现雾霾天气增多现象,下列不属于大气污染物的是( )
| A. | 可吸入颗粒物(PM2.5) | B. | CO2 | ||
| C. | NO2 | D. | SO2 |
1. 观察水电解微观示意图,从不同角度进行分析,写出你从宏观、微观方面所获取的信息.
观察水电解微观示意图,从不同角度进行分析,写出你从宏观、微观方面所获取的信息.
 观察水电解微观示意图,从不同角度进行分析,写出你从宏观、微观方面所获取的信息.
观察水电解微观示意图,从不同角度进行分析,写出你从宏观、微观方面所获取的信息.| 不同角度 | 我的理解 | |
| A | 物质的组成 | 水是由氢、氧元素组成 |
| B | 分子的构成 | 每个水分子由2个氢原子和1个氧原子构成 |
| C | 物质的变化 | 水在通电时分解生成了氢气和氧气 |
| D | 化学反应的过程 | 分子分成原子,原子重新组合 |
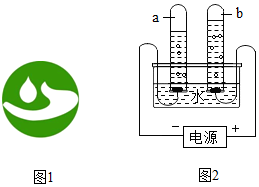 2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请回答下列问题:
2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请回答下列问题: