题目内容
19.(1)如图1是初中化学中的一些重要实验.请回答:
①A是氢气或甲烷的燃烧实验,点燃前必须检验纯度;
②B实验中能够说明盐酸与氢氧化钠发生了反应的现象是溶液由红色变为无色;
③C是除去粗盐中难溶性杂质实验中的过滤操作,过滤后发现滤液仍然浑浊,其可能的原因是滤纸破损(或滤液边缘高于滤纸边缘、仪器不干净等)(答出一种原因即可).
(2)如图2所示是A、B、C三种物质的溶解度曲线,据此图回答:
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A;
②t2℃时,将30gA放入100g水中,充分搅拌后,所得溶液的溶质质量分数是20%;
③t3℃时,将等质量A、B两种物质的饱和溶液降温到t2℃时,析出晶体质量较大的是A;
④t3℃时,将25gC放入100g水中,充分搅拌后得到C的饱和溶液,在不改变溶剂量的前提下,将其变为不饱和溶液的方法是降温至低于t2℃.
分析 (1)①根据可燃性气体与空气混合后点燃可能发生爆炸进行分析解答.
②稀盐酸和氢氧化钠溶液恰好完全反应时溶液呈中性,当酚酞试液变为无色说明发生了反应.
③根据过滤操作中玻璃棒的作用进行分析解答;凡是不经滤纸的过滤就直接进入滤液的操作,都能造成滤液浑浊;另外接滤液的烧杯不干净也会造成同样的结果;
(2)①据溶解度曲线可比较同一温度下不同物质的溶解度大小;
②根据t2℃时A物质的溶解度来分析;
③根据两种物质的溶解度受温度的影响情况来分析;
④据C的溶解度随温度变化情况分析解答.
解答 解:(1)①氢气或甲烷具有可燃性,与空气混合遇明火可能发生爆炸,为防止发生爆炸,点燃前必须检验纯度;故填:检验纯度;
②氢氧化钠溶液显碱性,能使酚酞试液变红色;氢氧化钠与盐酸恰好完全反应时,溶液呈中性,此时酚酞溶液显无色,故当溶液由红色变为无色时,说明氢氧化钠与盐酸发生了反应.故填:溶液由红色变为无色;
③过滤后滤液仍浑浊,可能原因是滤纸破损(会使得液体中的不溶物进入下面的烧杯,从而使得滤液浑浊)、液面高于滤纸边缘(会使部分液体未经过滤纸的过滤直接流下,该操作会使滤液仍然浑浊)或盛接滤液的烧杯不干净等.故填:滤纸破损(或滤液边缘高于滤纸边缘、仪器不干净等);
(2)①t1℃时,三种物质溶解度从大到小顺序为 C>B>A;故填:C>B>A;
②t2℃时,A物质的溶解度为25g,也就是在该温度下,100g水中最多溶解25gA就达到饱和状态,故此时将30gA物质放入100g水中不能完全溶解,只溶解了25g,此饱和溶液中溶质的质量分数为:$\frac{25g}{25g+100g}×100%$=20%,故填:20%;
③t3℃~t2℃,A的溶解度变化幅度比B大,所以将等质量A、B两种物质的饱和溶液降温到t2℃时,析出晶体质量较大的是A;故填:A;
④饱和溶液变为不饱和溶液的一般方法是降温、蒸发溶剂,C的溶解度随温度的降低而增大,t3℃时,将25gC放入100g水中,充分搅拌后得到C的饱和溶液,要在不改变溶剂量的前提下,将其变为不饱和溶液,应采取降温的方法,t2℃时,C的溶解度是25g,即降温至t2℃时恰好饱和,所以应降至t2℃时以下;
故填:降温至低于t2℃.
点评 本题主要考查了学生对溶解度概念的认识、溶质质量分数的考查、重点是溶解度曲线的意义的应用,能很好考查学生对知识的理解和应用.

| A. | 配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌 | |
| B. | 纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 | |
| C. | 用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 | |
| D. | 汽车或电动车的蓄电池中用到的硫酸溶液时由浓硫酸稀释而成的 |
 如图是某化学反应的微观模型,“○”、“●”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
如图是某化学反应的微观模型,“○”、“●”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 反应中原子的个数没有变 | |
| D. | 参加反应的两种分子个数之比为3:2 |
| 元 素 | X | Y | Z |
| 相关信息 | 其单质甲是一种清洁能源 | 地壳中含量最多的元素 | 其一种单质是天然存在的最硬的物质 |
(2)写出元素X与Z形成的化合物的化学式CH4.
(3)写出X与Y的单质在点燃条件下反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(4)写出ZY→ZY2之间转化的化学方程式:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
| A. | 组成元素相同的物质其化学性质一定相同 | |
| B. | 同温下,同种溶质的饱和溶液一定比不饱和溶液的浓度大 | |
| C. | 饱和溶液降低温度一定会析出晶体 | |
| D. | 质子数相同的两种粒子其核外电子数一定相等 |
| A. | 用石墨做电极 | B. | 用Ca(OH)2改良酸性土壤 | ||
| C. | 用金刚石做钻头 | D. | 用铝做成门窗 |
| A. | 钠不能保存在水中 | |
| B. | 将石蕊试液滴入钠与水反应后的溶液中会变为蓝色 | |
| C. | 不能用手直接拿金属钠 | |
| D. | 将钠投入硫酸铜溶液中会析出红色物质 |
| A. | 看外观 | |
| B. | 分别加入到少量水中,观察温度的变化 | |
| C. | 分别称量 | |
| D. | 分别用小木条蘸取少量,观察木条是否变黑 |
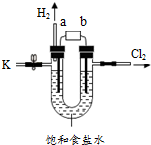 某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.
某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.资料:
1:电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
2:Cl2能溶于水.
探究活动一:确定电解饱和食盐水后的产物
(1)此电解原理与电解水原理类似,则a端为电源的负
极,甲组同学为了收集另一电极产生的气体,
他们用向上排空气法 法进行收集;
(2)甲组同学从K处取出一部分待测液,往里面加入
酚酞,发现溶液变红,说明电解后生成了氢氧化钠;
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取10g待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入溶质质量分数为19.6%的稀硫酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀硫酸的质量/g | 0 | 4.0 | 6.0 | 8.0 | 10.0 | 12.0 |
| 烧杯中溶液的pH | 13.0 | 12.8 | 12.5 | 12.3 | 7.0 | 1.3 |
(4)当加入6g稀硫酸时,溶液中溶质为氢氧化钠、硫酸钠,利用氢氧化钠与稀硫酸恰好完全反应时的实验数据,计算待测液中氢氧化钠的质量分数为16%;
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:

(5)步骤 ②加入的氯化镁溶液必须足量,其目的是使氢氧化钠完全反应;滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取少量反应后的待测溶液,滴加氢氧化钠;产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论);
(6)步骤 ③过滤出的沉淀物是氢氧化镁(填物质的名称);
(7)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所
测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).