题目内容
2.如图为元素周期表中某一周期元素的原子结构示意图.
请回答下列问题:
(1)表中磷原子的核电荷数x=15.
(2)表中具有相对稳定结构的元素是氩(Ar).
(3)一个铝离子的符号是Al3+,若某种铝原子的相对原子质量为27,则它的中子数为14.
(4)上述元素原子的共同点是核外电子层数相同.
分析 (1)根据原子中质子数=核外电子数,进行分析解答.
(2)最外层具有8个电子的原子具有相对稳定结构.
(3)根据铝原子最外层电子数为3,容易失去3个电子以及相对原子质量=质子数+中子数进行解答;
(4)根据元素周期数与电子层数的关系进行分析解答.
解答 解:(1)原子中质子数=核外电子数,则磷原子的核电荷数x=2+8+5=15.故填:15;
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.故填:氩(Ar);
(3)铝原子最外层电子数为3,容易失去3个电子;中子数=相对原子质量-质子数=27-13=14;故填:Al3+、14;
(4)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.故填:核外电子层数相同.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是正确解题的关键.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
12.下列说法正确的是( )
| A. | “釜底抽薪”是利用了隔绝空气的灭火原理 | |
| B. | 可燃物温度达到着火点即可燃烧 | |
| C. | 不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火 | |
| D. | 燃烧是人类最早利用的化学反应之一 |
13.下列过程发生化学变化的是( )
| A. | 石油分离出汽油、柴油 | B. | 煤转化为煤气 | ||
| C. | 铁水铸成零件 | D. | 利用金刚石裁玻璃 |
10.某同学的妈妈因病手术,医生嘱咐要增加摄入蛋白质类食物以利于伤口愈合.则他为妈妈准备的 以下食物中,最有利于伤口愈合的是( )
| A. | 苹果、香蕉 | B. | 牛奶、鸡蛋 | C. | 巧克力、橙汁 | D. | 面包、饼干 |
17.小明学习了金属活动性顺序后,欲进一步进行实验探究,他将一小块金属钠投入CuSO4溶液中,看到了下列现象:有大量气体产生,并出现了蓝色沉淀,但没有红色物质析出.小明通过查阅资料,发现钠能与水反应,于是又补做了另一个实验,并记录如下:
分析:由上述现象可知:金属钠与水反应后,生成物中呈碱性的物质是NaOH(选填“NaOH”或“Na2CO3”),其理由是反应物中没有碳元素.
结论:据上述现象,Na投入CuSO4溶液中产生的蓝色沉淀是Cu(OH)2.
反思:按金属活动性顺序,一种活动性较强的金属不一定能(选填“能”、“不能”、“不一定能”)把另一种活动性较弱的金属从它的盐溶液中置换出来.
| 操作步骤 | 实验现象 |
| ①将一小块钠放入盛水的烧杯中 | 金属钠在水面四处游动,并逐渐溶解,有大量气体产生 |
| ②向反应后的溶液中滴加酚酞试液 | 溶液变红色 |
| ③将产生的气体收集并点燃 | 气体燃烧,并产生淡蓝色火焰 |
结论:据上述现象,Na投入CuSO4溶液中产生的蓝色沉淀是Cu(OH)2.
反思:按金属活动性顺序,一种活动性较强的金属不一定能(选填“能”、“不能”、“不一定能”)把另一种活动性较弱的金属从它的盐溶液中置换出来.
7.下表是三种气体的密度(在0℃、101Kpa条件下测定)和溶解度(20℃、101Kpa条件下测定).实验室要收集SO2气体:可采取的方法是( )
| H2 | CO2 | SO2 | |
| 密度(g/L) | 0.08987 | 1.975 | 2.716 |
| 溶解度(g) | 0.0001603 | 0.1688 | 11.28 |
| A. | 向上排空气法 | B. | 向下排空气法 | ||
| C. | 排水集气法 | D. | 向下排空气法和排水法都可以 |
14. 碳的耗用量称为“碳足迹”.一般情况下,排放的二氧化碳越多,“碳足迹”就越大.“碳足迹”的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗品.以下做法可以减小“碳足迹”的是( )
碳的耗用量称为“碳足迹”.一般情况下,排放的二氧化碳越多,“碳足迹”就越大.“碳足迹”的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗品.以下做法可以减小“碳足迹”的是( )
 碳的耗用量称为“碳足迹”.一般情况下,排放的二氧化碳越多,“碳足迹”就越大.“碳足迹”的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗品.以下做法可以减小“碳足迹”的是( )
碳的耗用量称为“碳足迹”.一般情况下,排放的二氧化碳越多,“碳足迹”就越大.“碳足迹”的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗品.以下做法可以减小“碳足迹”的是( )| A. | 生活垃圾就地焚烧处理 | B. | 大量使用煤、石油等燃料 | ||
| C. | 减少一次性筷子的使用 | D. | 以私家车出行代替公共交通工具 |
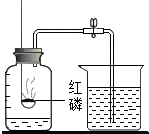 如图是测定空气中氧气含量的实验装置,请回答下列问题:
如图是测定空气中氧气含量的实验装置,请回答下列问题: