题目内容
7.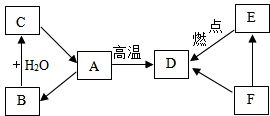 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为金属氧化物;D、E、F三种物质含有同种非金属元素,E是易与血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去).试回答:
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为金属氧化物;D、E、F三种物质含有同种非金属元素,E是易与血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去).试回答:(1)C的名称:氢氧化钙;
(2)用化学方程式表示E在工业炼铁中的用途:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)A→D的基本反应类型分解反应.
分析 根据题意,A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,大理石的主要成分是碳酸钙,则该金属元素是钙元素;B为金属氧化物,则B为氧化钙;氧化钙与水反应生成氢氧化钙,则C为氢氧化钙.D、E、F三种物质含有同种非金属元素,E是易与血液中血红蛋白结合的有毒气体,则E为一氧化碳,一氧化碳燃烧生成二氧化碳,则D为二氧化碳;F可能是碳或氧气;据此进行分析解答.
解答 解:A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,大理石的主要成分是碳酸钙,则该金属元素是钙元素;B为金属氧化物,则B为氧化钙;氧化钙与水反应生成氢氧化钙,则C为氢氧化钙.D、E、F三种物质含有同种非金属元素,E是易与血液中血红蛋白结合的有毒气体,则E为一氧化碳,一氧化碳燃烧生成二氧化碳,则D为二氧化碳;F可能是碳或氧气.
(1)C的名称是氢氧化钙.
(2)E在工业炼铁中的用途,即工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)A→D,即碳酸钙高温分解生成氧化钙和二氧化碳,该反应符合“一变多”的特征,属于分解反应.
故答案为:(1)氢氧化钙;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)分解反应.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.PM2.5是造成雾霾天气“元凶”之一,下列做法不会增加空气中的PM2.5的是( )
| A. | 工厂排放烟尘 | B. | 外出时佩戴防雾霾口罩 | ||
| C. | 燃放鞭炮 | D. | 焚烧秸秆 |
18.通过化学学习,我们了解了生活中物质变化的本质.下列变化中与其它不同的是( )
| A. | 木柴劈成块 | B. | 西瓜榨成汁 | C. | 海水晒盐 | D. | 米饭变馊 |
15.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )
| A. | 滤渣中一定有银、没有铜和锌 | |
| B. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| C. | 滤渣中一定有银和锌,可能有铜 | |
| D. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 |
2.下列离子在同一溶液中能大量共存的是( )
| A. | Na+、CO32-、SO42-、H+ | B. | K+、OH-、Na+、Cl- | ||
| C. | Mg2+、K+、OH-、NO3- | D. | Ba2+、H+、SO42-、Cl- |
12.下列事故的处理方法错误的是( )
| A. | 炒菜时,油锅着火,立即盖上锅盖 | |
| B. | 图书室内文字资料起火,立即用泡沫灭火器灭火 | |
| C. | 发生一氧化碳中毒,立即转移到通风的地方救治 | |
| D. | 实验时如果不慎将浓硫酸沾到皮肤上,立即用干布抹去,再用大量水冲洗 |
19.下列物质鉴别的实验方法错误的是( )
| 选项 | 鉴别的物质 | 实验方法及现象 |
| A | 铁和锌 | 滴加稀盐酸,观察是否产生气泡 |
| B | 食盐和纯碱 | 滴加食醋,观察是否产生气泡 |
| C | 过氧化氢和蒸馏水 | 加入二氧化锰,观察是否产生气泡 |
| D | 碳酸氢铵和硫酸铵 | 滴加稀盐酸,观察是否产生气泡 |
| A. | A | B. | B | C. | C | D. | D |