题目内容
2.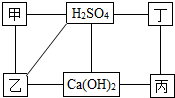 如图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.请回答:
如图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.请回答:(1)写出乙和丙的化学式:
乙Na2CO3,丙HCl;
(2)写出甲和乙反应的化学方程式:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3;
(3)丙和丁反应的现象为银白色固体表面冒大量气泡,固体逐渐减少,放大量热.
分析 根据物质的性质结合框图找突破口,由酸的五点通性,硫酸与甲、乙、丁反应,而不与丙反应,推出丙为HCl,由氢氧化钙与乙反应,推出乙为Na2CO3,而甲与乙反应,甲为Ba(NO3)2,丁为Mg,然后进行验证即可.
解答 解:(1)在给定的转化关系中,硫酸与甲、乙、丁三种物质反应,而甲、乙、丙、丁(Mg、BaCl2、Na2CO3、HCl)中只有HCl不和硫酸反应,所以丙为HCl;由氢氧化钙与乙反应,推出乙为Na2CO3,而甲与乙反应,甲为Ba(NO3)2,丁为Mg,乙是Na2CO3;
(2)硝酸钡和碳酸钠反应生成碳酸钡和硝酸钠,化学方程式为:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3,(3)镁和HCl溶液反应生成氯化镁和氢气,化学方程式为:Mg+2HCl═MgCl2+H2 ↑.故丙和丁反应的现象为银白色固体表面冒大量气泡,固体逐渐减少,放大量热.
故答案为:
(1)Na2CO3; HCl;(2)Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3;
(3)银白色固体表面冒大量气泡,固体逐渐减少,放大量热.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
13.下列关于微粒的说法错误的是( )
| A. | 在原子中,电子的质量很小,可以忽略,故原子的质量主要集中在原子核上 | |
| B. | 分子和原子都可以直接构成物质,而阳离子与阴离子却不能单独构成物质 | |
| C. | 构成物质的分子在不断的运动,而构成物质的原子却固定不动 | |
| D. | 在离子化合物中,阳离子所带正电荷之和等于阴离子所带负电荷之和 |
17. 液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
 液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )| A. | 丙烷是由3个碳原子和8个氢原子构成的 | |
| B. | 丙烷中碳、氢元素的质量比为3:8 | |
| C. | 一个丙烷分子中有26个电子 | |
| D. | 丙烷属于无机化合物 |
7.下列物质由原子构成的是( )
| A. | 铜 | B. | 氧气 | C. | 水 | D. | 氯化钠 |
14.分别将下列各组物质同时加入水中,仅得到无色透明溶液的是( )
| A. | HCl Na2SO4 KCl | B. | K2SO4 HCl Ba(OH)2 | ||
| C. | NaCl BaCO3 KNO3 | D. | FeCl3 KOH NaCl |
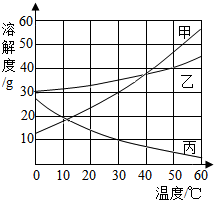 甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:
甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题: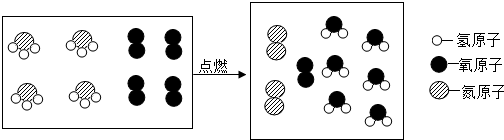
 四种粒子的个数比是4:3:2:6.
四种粒子的个数比是4:3:2:6.