题目内容
8.20℃时,NaCl溶解于水的实验数据如表.则下列叙述正确的是( )| 实验序号 | ① | ② | ③ | ④ |
| 水的质量(g) | 10 | 10 | 10 | 10 |
| 加入NaCl的质量(g) | 2 | 3 | 4 | 5 |
| 所得溶液的质量(g) | 12 | 13 | 13.6 | 13.6 |
| A. | ①所得溶液溶质质量分数为20% | |
| B. | ②所得溶液为饱和溶液 | |
| C. | 氯化钠属于可溶性固体 | |
| D. | 所得溶液的溶质质量分数大小关系为:④=③>②>① |
分析 由表中数据可知,随着氯化钠的不断加入,溶液的质量在增加,当10g水中溶解了3.6g氯化钠后不再溶解,说明已经达到饱和状态.
解答 解:A、①所得溶液的溶质质量分数为:$\frac{2g}{10g+2g}$×100%≈17%,故选项错误;
B、20℃时10g水最多能溶解3.6gNaCl,而②20℃时10g溶解了3g氯化钠,所以是不饱和溶液,故选项错误.
C、20℃时10g水最多能溶解3.6gNaCl,则其溶解度是36g,所以氯化钠属于易溶性固体,故选项错误;
D、因③④都是同温度下同种溶质的饱和溶液,则溶质的质量分数相等,①②都是不饱和溶液,溶质越多溶质的质量分数就大,则②>①,又同温度同溶质的饱和溶液是溶质溶解的最大极限,则饱和溶液中溶质的质量分数大于不饱和溶液中的溶质质量分数,则④=③>②>①,故选项正确.
故选:D.
点评 本题主要考查不饱和溶液和饱和溶液方面的知识,解答时要紧紧围绕表中数据进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
18.向Al(NO3)3、AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤出的固体中滴加稀盐酸时,有气泡产生.则滤液中含有的金属离子有( )
| A. | Ag+ | B. | Al3+、Ag+、Zn2+ | C. | Al3+、Zn2+ | D. | Ag+、Zn2+ |
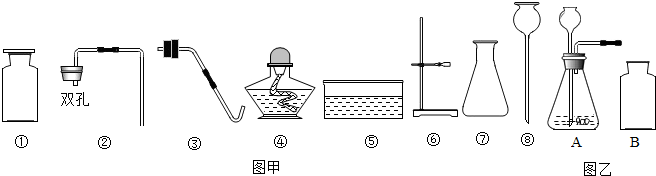
3.看图回答下列问题:
(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色.判断:①A中产生的气体是氢气.C中的氧化铜由黑色变为红色,反应前后(用符号填充)H,Cu元素的化合价发生了变化.
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
①写出实验室制CO2的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
| A | B | C | D | E | F | |
| 装置图 | 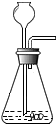 | 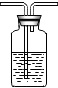 | 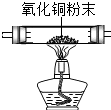 | 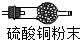 | 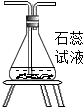 | 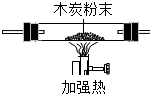 |
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
| 实验 要求 | 制CO2 | 证明CO2与H2O化合 | CO2→CO | CO还原性 | 除去混和气体 |
| 装置 编号 | A | E | F | C | B |
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
20.为了测定某石灰石样品的纯度,实验室取15克石灰石样品,向其中分3次加入共150g某浓度稀盐酸,实验数据如下表:(杂质不与稀盐酸反应)
计算:
(1)m=2.2;
(2)石灰石的纯度?
(3)所用稀盐酸的溶质的质量分数?
| 实验 | 第一次 | 第二次 | 第三次 |
| 稀盐酸的质量 | 50克 | 50克 | 50克 |
| 收集到的气体的质量 | 2.2克 | m克 | 1.1克 |
(1)m=2.2;
(2)石灰石的纯度?
(3)所用稀盐酸的溶质的质量分数?
8.物质性质决定用途.下列说法错误的是( )
| A. | 熟石灰具有碱性,和硫酸铵混合使用防止土壤酸化、板结 | |
| B. | 小苏打具有弱碱性,可用于治疗胃酸过多 | |
| C. | 硫酸铜溶液能与铁反应,切割钢板时用于划线 | |
| D. | 镁能在空气中燃烧发出耀眼的白光,可用于制造照明弹 |