题目内容
14.通过化学学习,你已经掌握了实验室制取气体的有关规律,如图是老师提供的一些实验装置.请结合如图回答问题:
(1)实验室中常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,应选择的发生装置是B;已知氨气极易溶于水,则收集氨气应选择的装置是D.
(2)反应过程中除了生成氨气外还生成氯化钙和水蒸气,请写出该反应的化学方程式:2NH4C1+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)将干燥的氨气通入F装置中,反应一段时间后发现黑色粉末逐渐变成了红色,可见氨气具有还原性性,氨气和该黑色粉末反应时除了生成红色粉末还生成了空气中含量最高的物质和另一种物质,请写出该反应的化学方程式3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
(4)某同学欲在实验室制取并收集一瓶干燥的氨气,同时探究氨气能否与CuO反应,则接口的连接顺序为:b连接g,h连接f,e连接i.
(5)氨气对空气会造成一定的污染,从环保角度考虑,还需对以上装置进行改进,请简述改进措施.
(6)某工厂变废为宝,探究用废硫酸等来制取所需产品.现有废硫酸14.7t(H2SO4的质量分数为20%),与足量废铁屑反应来制取硫酸亚铁,同时将生成的全部氢气在催化剂的作用下,经过高温高压与足量的氮气化合生成氨气,理论上可以生产多少氨气.
分析 (1)根据若用加热氯化铵和氢氧化钙的固体混合物的方法制取氨气,应选择的发生装置是需要加热的,因为氨气密度比空气小,极易溶于水,因此收集装置是:向下排空气法解答;
(2)根据氯化铵和氢氧化钙反应,写出化学方程式;
(3)根据氨气具有还原性,利用题中信息写出反应的化学方程式;
(4)根据实验室中常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,应选择的发生装置是B;用碱石灰进行干燥解答;
(5)氨气对空气会造成一定的污染,不能直接排放到空气直接;
(6)根据化学反应方程式中的已知物质的质量来求未知物质的质量.
解答 解:
(1)若用加热氯化铵和氢氧化钙的固体混合物的方法制取氨气,应选择的发生装置是需要加热的,因为氨气密度比空气小,极易溶于水,因此收集装置是:向下排空气法;
(2)氯化铵和氢氧化钙反应的化学方程式为:2NH4C1+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)将干燥的氨气通入F装置中,反应一段时间后发现黑色粉末逐渐变成了红色,可见氨气具有还原性;利用质量守恒定律写出化学方程式为:
3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(4)某同学欲在实验室制取并收集一瓶干燥的氨气,同时探究氨气能否与CuO反应,实验室中常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,应选择的发生装置是B;用碱石灰进行干燥,用D收集,则接口的连接顺序为:b连接g,h连接f,e连接i;
(5)氨气对空气会造成一定的污染,该装置中缺少了尾气处理装置.将尾气进行收集等,防止氨气污染空气.
(6)根据两个方程式:Fe+H2SO4═FeSO4+H2↑ 和N2+3H2 $\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$2NH3分析出:硫酸、氢气与铜之间的质量关系,然后利用硫酸的质量来计算出铜的质量即可.
设理论上最多可生产铜的质量为x.
因为:Fe+H2SO4═FeSO4+H2↑ 和N2+3H2 $\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$2NH3
可得关系式:3H2SO4~3H2~2NH3
294 34
14.7t×20% x
$\frac{294}{14.7t×20%}=\frac{34}{x}$
x=0.34t
答案:
(1)B D
(2)2NH4C1+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(3)还原性 3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O
(4)b g h f e i
(5)将尾气进行收集
(6)理论上可以生产0.34t氨气.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和碱的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中

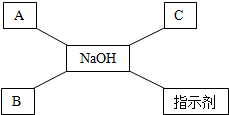 如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,C是人体胃液中的酸,“-”表示相连两物质之间能相互反应.下列说法错误的是( )
如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,C是人体胃液中的酸,“-”表示相连两物质之间能相互反应.下列说法错误的是( )| A. | 若指示剂是紫色石蕊,则紫色石蕊遇氢氧化钠溶液变成蓝色 | |
| B. | A物质与氢氧化钠溶液反应有白色沉淀产生 | |
| C. | B物质可能是二氧化碳 | |
| D. | C物质与氢氧化钠发生的是中和反应 |
| A. | 在化学变化中分子可以分成原子 | |
| B. | 氯化钠是由氯化钠离子构成 | |
| C. | 构成物质的粒子有分子、原子、离子等 | |
| D. | 氧化物中一定含有氧元素 |
| A. | 用带火星的木条伸入瓶内检验O2是否集满 | |
| B. | 用适量的水能区分NH4NO3固体和NaOH固体 | |
| C. | 粗盐提纯实验中,蒸发结晶直到滤液蒸干时停止加热 | |
| D. | 用pH试纸测定溶液酸碱度时,先将pH试纸用水润湿,然后再测定 |
| A. | 蒜蓉茼蒿 | B. | 酱香肉包 | C. | 油炸小鲫鱼 | D. | 香煎豆腐 |