题目内容
20.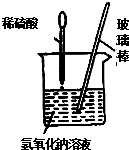 为研究中和反应,某科学兴趣小组同学用稀H2SO4和NaOH溶液反应进行了实验.
为研究中和反应,某科学兴趣小组同学用稀H2SO4和NaOH溶液反应进行了实验.(1)为确定两种物质是否刚好中和,小刚取出一定量反应后的溶液于试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.小华认为小刚的结论不正确,她认为除了“恰好中和”外,还有可能是稀硫酸过量.
(2)小华改进了小刚的实验,利用右图的装置,在烧杯中放入NaOH溶液和几滴酚酞试液,逐滴加入稀H2SO4,并用玻璃棒不断搅拌,当看到溶液红色未消失时,溶液中存在的离子是Na+ SO42- OH-.(填写离子符号)
分析 (1)根据酸性和中性的液体都不会使酚酞变色进行分析;
(2)根据溶液红色未消失,说明溶液显碱性氢氧化钠过量来分析.
解答 解:
(1)溶液中性或酸性时,都不会使酚酞变色,恰好完全反应时溶液显中性,稀硫酸过量时显酸性,故答案为:稀盐酸过量;
(2)在烧杯中放入NaOH溶液和几滴酚酞试液,逐滴加入稀H2SO4,并用玻璃棒不断搅拌,当看到溶液红色未消失,说明溶液显碱性氢氧化钠过量,故溶质含有氢氧化钠和生成的硫酸钠;溶液中存在的离子是Na+ SO42- OH-.
(1)稀硫酸过量; (2)Na+ SO42- OH-.
点评 解答本题时要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,同时要明确酸碱中和的性质,学会检验酸碱的方法,并注意方法的可行性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10. 某纯碱中含有少量氯化钠杂质,为检验其纯度,小周取出27g纯碱样品,平均分成五份,依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应、待气体充分溢出后,用天平称质量(如图),得到如表数据.请计算
某纯碱中含有少量氯化钠杂质,为检验其纯度,小周取出27g纯碱样品,平均分成五份,依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应、待气体充分溢出后,用天平称质量(如图),得到如表数据.请计算
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是2.2g.
(2)计算纯碱样品中碳酸钠的质量分数是多少?(精确到0.1%)
(3)关于所用稀盐酸的质量分数,三位同学做法各不相同(如图).判断谁的做法正确,并分析另两位同学的错误之处.

 某纯碱中含有少量氯化钠杂质,为检验其纯度,小周取出27g纯碱样品,平均分成五份,依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应、待气体充分溢出后,用天平称质量(如图),得到如表数据.请计算
某纯碱中含有少量氯化钠杂质,为检验其纯度,小周取出27g纯碱样品,平均分成五份,依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应、待气体充分溢出后,用天平称质量(如图),得到如表数据.请计算| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 173.9 | 179.3 |
(2)计算纯碱样品中碳酸钠的质量分数是多少?(精确到0.1%)
(3)关于所用稀盐酸的质量分数,三位同学做法各不相同(如图).判断谁的做法正确,并分析另两位同学的错误之处.

11.实验室有两瓶标签脱落的溶液,只知道是盐酸溶液和氢氧化钠溶液.请从下列提供的试剂中选择一种试剂,用两种不同的方法将它们鉴别出来.
提供的试剂:①氧化铁 ②氢氧化钙 ③氯化钠溶液 ④氢氧化钡溶液 ⑤硫酸铜溶液
提供的试剂:①氧化铁 ②氢氧化钙 ③氯化钠溶液 ④氢氧化钡溶液 ⑤硫酸铜溶液
| 选择的试剂编号 | 有明显反应现象的化学方程式 | |
| 方法一 | ||
| 方法二 |
8.甲同学对实验室的“氢氧化钙是否变质以及变质的程度”展开了探究活动.
(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:
甲经过思考,认为样品存在三种可能情况:没有变质;部分变质;完全变质.
(3)实验探究:
(4)小结与思考:
根据上述实验现象,甲确定该样品已部分变质,请写出他在探究实验中发生反应的一个化学方程式:Ca(OH)2+2HCl=CaCl2+2H2O.
(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:
甲经过思考,认为样品存在三种可能情况:没有变质;部分变质;完全变质.
(3)实验探究:
| 实验步骤及操作 | 可能的实验现象 | 实验结论 |
| 取样于试管中,加入足量蒸馏水振荡后,静置; ①取上层清液,滴入无色酚酞试液; ②倒去上层清液,再向试管中滴加稀盐酸. | ①溶液变红;②有大量的气泡冒出. | 部分变质 |
| ①溶液不变色;②有大量的气泡冒出. | 全部变质 | |
| ①无色酚酞试液变红;②没有气泡产生. | 没有变质 |
根据上述实验现象,甲确定该样品已部分变质,请写出他在探究实验中发生反应的一个化学方程式:Ca(OH)2+2HCl=CaCl2+2H2O.
15.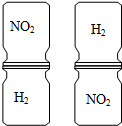 把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
 把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )
把红棕色的NO2气体和无色的H2的集气瓶,按如图两种方式放置,然后抽去两瓶之间的玻璃片,可观察到左边的两瓶气体的颜色很快趋于一致,右边的两瓶需较长时间才能达到同样的效果,由此现象不能得出的结论是( )| A. | 分子是在不断运动 | B. | 分子之间有间隔 | ||
| C. | 氢气的密度比二氧化氮小 | D. | 分子由原子构成 |
5.冰融化成水时,发生改变的是( )
| A. | 分子的种类 | B. | 分子间的间隔 | ||
| C. | 分子本身体积变大 | D. | 分子质量变小 |
12.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,经检验,滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2.
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家一致认为猜想四不合理,其原因是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
实验二中发生明显现象的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【反思与拓展】登山运动员常用CaH2作为能源提供剂,与氢气相比的优点是携带安全.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2.
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家一致认为猜想四不合理,其原因是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后产生气泡 | 猜想三成立 |
【反思与拓展】登山运动员常用CaH2作为能源提供剂,与氢气相比的优点是携带安全.
9.为探究NaCl和CuSO4对唾液淀粉酶活性的影响,某同学进行了实验,实验步骤和结果见表.
(1)实验中加入缓冲液的作用是维持反应液中pH的稳定.
(2)分析实验结果可知:对酶活性有影响的离子是Cl-和Cu2+,其中对酶活性有抑制作用的离子是Cu2+,对酶活性有促进作用的离子是C1-.
(3)该实验中设置4号试管的目的是对照; 设置3号试管的目的是确定Na+和SO42-对唾液淀粉酶的活性是否有影响.
| 试管编号 实验步骤 | 1 | 2 | 3 | 4 |
| 1%NaCl溶液(mL) | 1 | |||
| 1% CuSO4溶液(mL) | 1 | |||
| 1% Na2SO4溶液(mL) | 1 | |||
| 蒸馏水(mL) | 1 | |||
| pH6.8缓冲液(mL) | 1 | 1 | 1 | 1 |
| 1%淀粉溶液(mL) | 1 | 1 | 1 | 1 |
| 唾液淀粉酶溶液(mL) | 1 | 1 | 1 | 1 |
| 各试管放入37℃恒温水浴保温适宜时间 | ||||
| 取出试管,加入1%碘溶液0.1mL | ||||
| 观察结果 | 无色 | 深蓝色 | 浅蓝色 | |
(2)分析实验结果可知:对酶活性有影响的离子是Cl-和Cu2+,其中对酶活性有抑制作用的离子是Cu2+,对酶活性有促进作用的离子是C1-.
(3)该实验中设置4号试管的目的是对照; 设置3号试管的目的是确定Na+和SO42-对唾液淀粉酶的活性是否有影响.
10.钙是人体必须的常量元素,为保持体内钙元素的量,青少年与中老年都需要“补钙”.如图是某钙片的部分说明书.请回答下列问题:
(1)写出该钙片中含有人体所需七大营养素中的两种钙元素和维生素.
(2)CaCO3中钙元素的质量分数为多大?
(3)若每片此钙片的质量为1g,按用量服用,每天摄入钙元素的质量为多少克?
| ×××钙片 [药品规格]每片含CaCO3 0.625g,维生素D100国际单位. [用法用量]每次1片,每天2次 |
(2)CaCO3中钙元素的质量分数为多大?
(3)若每片此钙片的质量为1g,按用量服用,每天摄入钙元素的质量为多少克?