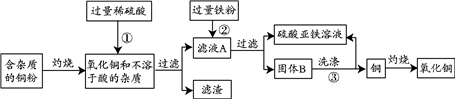
题目内容
9.将过量的铁粉放入一定量的硫酸铜溶液中(已知Fe+CuSO4=Cu+FeSO4),下列图象能正确表示物质的数量关系的是( )| A. |  | B. |  | C. |  | D. |  |
分析 溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,再根据反应的化学方程式及其质量关系可以判断相关方面的问题.
解答 解:A、铁和硫酸铜反应的化学方程式及其质量关系为:
Fe+CuSO4=Cu+FeSO4,
56 64
由质量关系可知,随着反应的进行,硫酸亚铁质量逐渐增大,而当56份质量的铁形成溶液的一部分时析出64份质量的铜,即随着反应的进行,溶液质量逐渐减小,因此随着反应进行,硫酸亚铁质量分数逐渐增大,当硫酸铜完全反应后,硫酸亚铁质量分数不再变化,该选项对应关系正确;
B、当硫酸铜完全反应后,硫酸铜的质量分数减小到0,该选项对应关系不正确;
C、当56份质量的铁形成溶液的一部分时析出64份质量的铜,即随着反应的进行,溶液质量逐渐减小,该选项对应关系不正确;
D、当56份质量的铁形成溶液的一部分时析出64份质量的铜,即随着反应的进行,固体质量逐渐增大,当硫酸铜完全反应后,固体质量不再变化,该选项对应关系不正确.
故选:A.
点评 要会利用金属活动顺序表分析实验,前边的金属会把后边的金属从其盐溶液中置换出来,并且能够根据化学方程式及其反应物、生成物的质量关系进行正确的分析和判断.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
19.冬至到了,过年的脚步进了,农村家家户户都有熏香肠、腊肉的习惯,从而导致了雾霾天气更加严重.下列不属于大气污染物的是( )
| A. | PM2.5 | B. | CO2 | C. | SO2 | D. | NO2 |
20. 现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
 现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )| A. | 金属X、Y的活动性关系为:X>Y | |
| B. | t1时消耗稀盐酸的质量:X=Y | |
| C. | 若反应生成XCl2和YCl2,则X、Y的相对原子质量大小关系为:X<Y | |
| D. | t1时烧杯中溶液的质量:X<Y |
14.类推是化学学习中常用的思维方法,以下类推结果正确的是( )
| A. | 氧化物一定含有氧元素,所以HNO3一定是氧化物 | |
| B. | 有机物都含碳元素,所以含碳元素的化合物都是有机物 | |
| C. | H2点燃前必须验纯,则CO点燃前也必须验纯 | |
| D. | 分子可以构成物质,所以物质一定由分子构成 |
1.下列实验操作正确的是( )
| A. | 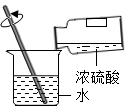 | B. | 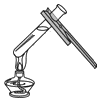 | C. |  | D. | 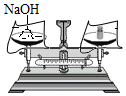 |
18.下列物质对应的化学式书写正确的是( )
| A. | 氯化铝 AlCl | B. | 氧化钠 NaO | C. | 硫酸铁 FeSO4 | D. | 硝酸镁 Mg(NO3)2 |
19.下列关于环境、资源的说法错误的是( )
| A. | 燃放鞭炮、“烧纸”等会增大雾霾的危害 | |
| B. | “白色污染”是指白色粉尘的污染 | |
| C. | 废弃的电脑等会产生镉、汞等有毒金属 | |
| D. | 废旧钢铁回收冶炼可提高资源的利用率 |