题目内容
15.下列化学方程式正确的是( )| A. | 2H2O2═2H2O+O2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | 2CO+Fe2O3═2Fe+2CO2 | D. | Fe2O3+6HCl═2FeCl2+3H2O |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、过氧化氢在二氧化锰的催化作用下生成水和氧气,正确的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
B、该化学方程式书写完全正确.
C、该化学方程式缺少反应条件,配平错误,正确的化学方程式应为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
D、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
故选:B.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
相关题目
3.下列关于实验操作或实验现象的描述正确的是( )
| A. | 测定未知溶液的酸碱度时,可以将pH试纸直接伸到待测溶液中 | |
| B. | 将氢氧化钠固体放在托盘天平的左盘滤纸上称量 | |
| C. | 如果皮肤上不慎沾上浓硫酸,应立即用大量的NaOH稀溶液冲洗 | |
| D. | 油脂易使人发胖,故我们要少食用含油脂的食物 |
20.下列关于物质分类的说法正确的是( )
| A. | 导电的物质都是金属 | B. | 有一定熔点的固体都是晶体 | ||
| C. | 橡胶、塑料都是合成材料 | D. | 含氧元素的化合物都是氧化物 |
4.下列叙述中正确的是( )
| A. | 不需要加热就能发生的变化是物理变化 | |
| B. | 物质燃烧时发生的化学变化 | |
| C. | 伴有发光、发热现象的变化一定是化学变化 | |
| D. | 需要加热才能发生的变化是化学变化 |
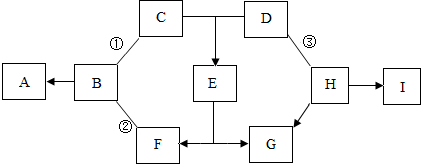
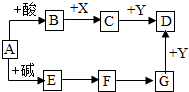 如图是初中化学常见物质间的转化关系(反应条件和部分产物已略),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态,请回答下列问题:
如图是初中化学常见物质间的转化关系(反应条件和部分产物已略),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态,请回答下列问题: