题目内容
18. 某化肥碳酸氢铵(NH4HCO3)的企业,作了一个如图所示的户外广告.
某化肥碳酸氢铵(NH4HCO3)的企业,作了一个如图所示的户外广告.(1)小明同学通过计算判断该广告属虚假广告,其理由是广告中含氮量为24%,大于碳酸氢铵中的含氮量17.7%.
(2)质量监督部门经过检测发现该化肥的含氮量为17.5%,则其中NH4HCO3的质量分数为98.87%.
(3)列式计算:多少千克的硝酸铵(NH4NO3)和这袋化肥的含氮量相当?
分析 (1)根据化合物中元素的质量分数进行分析;
(2)根据纯度的计算方法来分析;
(3)根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析.
解答 解:(1)碳酸氢铵中氮元素的质量分数为:$\frac{14}{79}×100%$100%=17.7%.故填:广告中含氮量为24%,大于碳酸氢铵中的含氮量17.7%.
(2)NH4HCO3的质量分数为:$\frac{17.5%}{17.7%}×100%$=98.87%.故填:98.87%.
(3)设质量为x的硝酸铵(NH4NO3)和这袋化肥的含氮量相当.$\frac{14×2}{80}$×100%×x=50kg×17.5%
解得x=25.0kg.
答:50.0千克的硝酸铵(NH4NO3)和这袋化肥的含氮量相当.
点评 此题是利用化学式的基础性计算,是对常规的计算的巩固与练习,抓准化学式是解题的关键.

练习册系列答案
相关题目
8.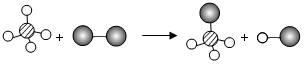 已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法正确的是( )
已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法正确的是( )
 已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法正确的是( )
已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法正确的是( )| A. | 图示中共有3种分子 | B. | 说明化学反应中原子不可分 | ||
| C. | 该图示不符合质量守恒定律 | D. | 该反应属于化合反应 |
13.“神州六号”的成功飞行极大地鼓舞了国人.作为发射飞船的火箭的推进器中盛有一种液态物质X和双氧水,当它们混合反应时,放出大量的热,产生强大推动力.有关的化学反应过程表示为:X+2H2O2═N2↑+4H2O,则X的化学式为( )
| A. | NH3 | B. | N2O4 | C. | NO2 | D. | N2H4 |
3.人们常把海水引入盐田,经风吹日晒水分蒸发获得粗盐,在这过程中海水中( )
| A. | 水的质量不变 | B. | 氯化钠的质量不变 | ||
| C. | 氯化钠溶液的质量分数始终不变 | D. | 氯化钠的质量变小 |
7. 2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
 2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )
2010年上海世博会标志性建筑之一中国馆“东方之冠”(如图)给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的核心筒.其中钢属于( )| A. | 金属或合金 | B. | 有机合成材料 | C. | 天然材料 | D. | 化合物 |
8.南阳硬玉的主要成分是NaAlSi2O6,下列关于该成分的说法正确的是( )
| A. | 其中Si是金属元素 | B. | 其中铝、氧元素的质量比为9:32 | ||
| C. | 由10个原子构成 | D. | 含有3个氧分子 |
