题目内容
9.根据以下各装置图回答问题:(所用装置图用序号表示)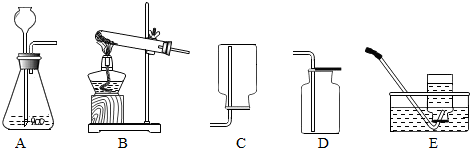
(1)写出图A中的两个实验仪器名称:锥形瓶和长颈漏斗.
(2)双氧水(H2O2的水溶液)在二氧化锰的催化作用下,能迅速分解出氧气,实验室里常用这种方法制取氧气.其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应属于分解反应(选填“化合反应”或“分解反应”).发生装置选用A,收集装置选用D或E,其中二氧化锰所起的作用是催化作用.
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,收集二氧化碳不能用E装置的原因是:二氧化碳可溶于水.
(4)在实验室中,常用加热固体NH4Cl和Ca(OH)2混合物的方法制取氨气,其反应的化学方程式为:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.已知在标准状况下,氨气的密度为0.77l g/L,空气的密度为l.293g/L,且在常温常压下,l体积水能溶解700体积的氨气.(氨气化学式NH3).则发生装置应选用B,收集装置应选用C.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气密度比空气大,不易溶于水,二氧化锰是该反应的催化剂进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,E装置是排水法收集进行分析;
(4)根据实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,易溶于水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,图A中的实验仪器有锥形瓶、长颈漏斗、导管等;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应满足分解反应一变多的条件,属于分解反应,过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气密度比空气大,不易溶于水,所以发生装置选用A,收集装置选用D,二氧化锰是该反应的催化剂,起催化作用;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,E装置是排水法收集,二氧化碳可溶于水,收集二氧化碳不能用排水法收集;
(4)实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,易溶于水,所以发生装置应选用B,收集装置应选用C.
故答案为:(1)锥形瓶,长颈漏斗等;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分解反应,A,D或E,催化作用;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑,二氧化碳可溶于水;
(4)B,C.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

A.淡蓝色 B.黑色 C.紫黑色 D.白色
| 物质 | 高锰酸钾固体 | 氧化镁 | 四氧化三铁 | 液氧 |
| 颜色 | C | D | B | A |
| A. | 洒在桌面上的酒精燃烧起来,立即用湿抹布盖灭 | |
| B. | 稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的小苏打溶液 | |
| C. | 碱液沾到皮肤上,用水冲洗后,再涂上硫酸溶液 | |
| D. | 少量酸滴到实验台上,应用湿抹布擦净,再用水冲洗抹布 |
| A. | 同种元素组成的物质一定是单质 | |
| B. | 同种原子构成的物质一定是单质 | |
| C. | 同种分子构成的物质一定是纯净物 | |
| D. | 质子数相同的粒子一定属于同种元素 |