题目内容
13.多角度认识物质的变化,有助于我们更好地理解化学知识.
(1)从微观角度,(图1为某化学反应的微观示意图,据图回答下列问题.)参加反应的A2与B2两种物质的分子个数比为1:1.
(2)从反应类型角度:在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和另一种单质,其反应的化学方程式为3C+2Fe2O3$\frac{\underline{\;一定条件\;}}{\;}$4Fe+3CO2或2C+Fe3O4$\frac{\underline{\;一定条件\;}}{\;}$3Fe+2CO2或C+2FeO$\frac{\underline{\;一定条件\;}}{\;}$2Fe+CO2.
(3)从能量变化角度看,(如图2实验装置分别进行下列实验,认识物质变化中的能力变化)往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是生石灰与水反应放出了大量的热,达到了白磷的着火点,
(4)如图3表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是氢离子和氢氧根离子(或H+和OH-)结合生成水.请写出一个与上述反应本质相同的化学反应方式:2KOH+H2SO4=K2SO4+2H2O.
分析 (1)根据微粒的变化分析分子原子的变化、参加反应的A2与B2两种物质的分子个数比;
(2)根据在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和另一种单质,写出反应的化学方程式;
(3)根据生石灰能与水反应放出热量分析回答;
(4)根据中和反应的实质和化学方程式的书写规则进行解答.
解答 解:(1)由化学反应的微观示意图可知,各种物质反应的微粒数目关系是: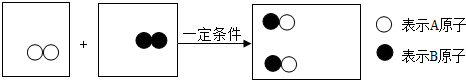
由上图可知,参加反应的A2与B2两种物质的分子个数比为1:1.
(2)在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和Fe.其反应的化学方程式为:3C+2Fe2O3$\frac{\underline{\;一定条件\;}}{\;}$4Fe+3CO2 或2C+Fe3O4$\frac{\underline{\;一定条件\;}}{\;}$3Fe+2CO2或C+2FeO$\frac{\underline{\;一定条件\;}}{\;}$2Fe+CO2
(3)往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是:生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.
(4)酸与碱反应的实质是氢离子和氢氧根离子结合成水的过程,例如:氢氧化钾和硫酸的反应化学方程式为:2KOH+H2SO4=K2SO4+2H2O;
答案:
(1)1:1;
(2)3C+2Fe2O3$\frac{\underline{\;一定条件\;}}{\;}$4Fe+3CO2 或2C+Fe3O4$\frac{\underline{\;一定条件\;}}{\;}$3Fe+2CO2或C+2FeO$\frac{\underline{\;一定条件\;}}{\;}$2Fe+CO2
(3)生石灰与水反应放出了大量的热,达到了白磷的着火点.
(4)氢离子和氢氧根离子(或H+和OH-);2KOH+H2SO4=K2SO4+2H2O(合理均可)
点评 通过本题的练习,学会从微观的角度认识物质及其变化,了解物质组成及变化的本质.当反应关系图存在干扰或者不是真正反应关系图时,将图转化为能够体现质量守恒定律的图,这样对解答起到很关键的作用.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
资料:①不同氢氧化物沉淀的pH范围:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
③高锰酸钾溶液只吸收SO2,不吸收CO2;
④碱溶液既吸收SO2,又吸收CO2. 试回答下列问题:
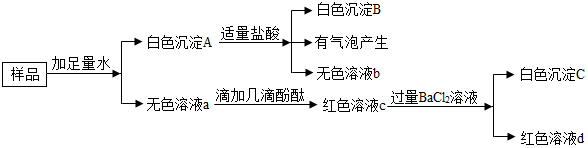
(1)MgCO3与稀硫酸反应的化学方程式为MgCO3+H2SO4═MgSO4+H2O+CO2↑.
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O.
(3)加氨水调节溶液的pH约为4的目的是使铁离子完全转化成氢氧化铁沉淀,反应的化学方程式为Fe2(SO4)3+6NH3•H2O=3(NH4)2SO4+2Fe(OH)3↓.
800℃
(4)煅烧过程存在以下反应:
2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集.(假设每步反应都完全进行)
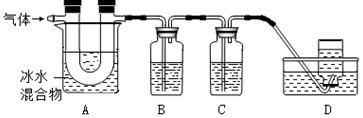
①A中现象是:玻璃管壁出现淡黄色固体;
②B中盛放的溶液可以是a(填字母),实验现象为产生沉淀;
a.Ca(OH)2 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③D中收集的气体是CO(填化学式).
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 点燃 |
| B | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铜粉 |
| C | 鉴别碳酸钙粉末和氯化钙粉末 | 加入稀盐酸 |
| D | 鉴别硬水和软水 | 加入活性炭 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 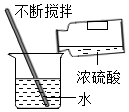 稀释浓硫酸 | B. | 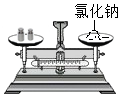 称取氯化钠 称取氯化钠 | C. |  过滤 | D. | 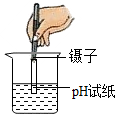 测溶液的pH 测溶液的pH |
| A. | 单质 | B. | 化合物 | C. | 氧化物 | D. | 混合物 |
| A. | 生石灰 | B. | 氧气 | C. | 葡萄糖 | D. | 烧碱 |

 .
.