题目内容
18.如图1是甲、乙、丙三种固体物质的溶解度曲线.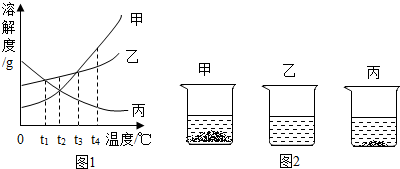
(1)t3℃时,将等质量的乙和丙分别配成饱和溶液,所用水的质量关系是乙<(填“>”、“<”或“=”).
(2)将t1℃时,甲和丙的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系是甲<(填“大于”、“小于”或“等于”)丙.
(3)20℃时,把等质量的甲、乙、丙三种固体分别加入到盛有50g水的烧杯中,充分溶解后,所得现象如图2,分析可知,20℃所处的温度范围是B(填字母).
A.0<20<t2 B.t1<20<t2 C.t2<20<t3
D.20>t3 E.以上都不对.
分析 (1)根据固体物质的溶解度曲线解答;
(2)根据在t2℃时,甲丙物质的溶解度解答;
(3)根据溶解度曲线可以判断物质的溶解度随温度的变化特点以及溶解度大小的关系,据此解答.
解答 解:(1)t3℃时,乙的溶解度大于丙,故将等质量的乙和丙分别配成饱和溶液,所用水的质量关系是乙<丙;
(2)据饱和时质量分数的计算式$\frac{溶解度}{100g+溶解度}$×100%可知:溶解度大则溶质的质量分数大,t1℃时甲丙的溶解度是:甲<丙,所以甲、丙两种物质的饱和溶液溶质的质量分数甲<丙;将t1℃的甲、丙两种物质的饱和溶液升温到t2℃时,甲溶液中溶质、溶剂的质量不变,溶质的质量分数不变,而丙的溶解度减小,会有晶体析出,但t2℃时丙的溶解度大于甲,故所得溶液中溶质质量分数的关系仍为为甲<丙.
(3)20℃时,把等质量的甲、乙、丙三种固体分别加入到盛有50g水的烧杯中,充分溶解后,所得现象如图2,分析可知,20℃时,三种物质的溶解度大小为乙>丙>甲,由图象可知:20℃所处的温度范围是t1<20<t2.
答案:(1)<;(2)<;(3)B
点评 本题难度不是很大,主要考查了固体溶解度曲线所表示的意义,并根据溶解度曲线解决相关的问题.掌握溶解度曲线的意义和应用是正确解答本题的关键.

练习册系列答案
相关题目
13.最近30多年,中国经济持续高速增长,但是今后的发展也面临着许多巨大的障碍,除了技术进步之外,最大障碍就是资源和环境因素,为了实现经济的可持续发展,下列说法正确的是( )
| A. | 为了提高粮食产量,农业上应多使用农药和化肥 | |
| B. | 将垃圾填坑改为露天焚烧,以减少土地的占用和对地下水的污染 | |
| C. | 推广新能源汽车,努力提高空气质量 | |
| D. | 为了提高居民健康水平,大力提倡长期饮用蒸馏水 |
3.下列物质中,与CO2、CuCl2溶液、FeCl3溶液都能发生反应,其都有明显现象的是( )
| A. | Ca(OH)2溶液 | B. | NaOH溶液 | C. | 稀盐酸 | D. | 稀硫酸 |
10.某元素在化合物中没有变价,相对原子质量为137,已知其氯化物的相对分子质量为208,则此元素形成的氧化物的相对分子质量是( )
| A. | 123 | B. | 153 | C. | 323 | D. | 336 |
17.某研究小组在学习氧气的化学性质时发现:大多数可燃物在空气中就能燃烧,而铁丝在空气中不能燃烧,在氧气中可以剧烈燃烧.该小组同学进行了下列探究.
【提出猜想】由以上事实可以做出以下猜想:
猜想一:可燃物燃烧的剧烈程度可能与氧气的浓度有关.
猜想二:可燃物燃烧的剧烈程度与可燃物的种类有关.(请补充完整)
【提出问题】可燃物的燃烧与氧气的浓度的大小有什么关系?
【查阅资料】在规定的条件下,物质在氧气、氮气混合气流中,维持稳定燃烧所需的最低氧气浓度(以氧气所占的体积百分数表示)叫氧指数.氧指数高表示材料不易燃,氧指数低表示材料容易燃烧.一般认为:氧指数<27%属易燃材料,27%≤氧指数<32%属可燃材料,氧指数≥32%属难燃材料.下面是一些常见物质氧指数.
【设计并实验】
(1)写出铁丝在氧气中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)由上表可知铁丝是难燃材料(填“易燃”“可燃”或“难燃”)
(3)在测定空气中氧气含量的实验中,我们通常选择红磷燃烧而不选择木炭或硫的原因是木炭或硫燃烧后的产物为气体.
【反思与评价】
(4)如果一定要用木炭代替红磷做这个实验,只要对实验稍作改进即可,需要对实验改进的是将蒸馏水改成氢氧化钠溶液;
理由是:氢氧化钠溶液对二氧化碳的吸收效果比蒸馏水好.
(5)即使这样的改进,根据上表数据可知:仍然没有用红磷燃烧好,原因是:木炭氧气含量在4%以下就不能燃烧了,而红磷仅仅到0.5%以下才不能燃烧,使得氧气反应更充分.
【提出猜想】由以上事实可以做出以下猜想:
猜想一:可燃物燃烧的剧烈程度可能与氧气的浓度有关.
猜想二:可燃物燃烧的剧烈程度与可燃物的种类有关.(请补充完整)
【提出问题】可燃物的燃烧与氧气的浓度的大小有什么关系?
【查阅资料】在规定的条件下,物质在氧气、氮气混合气流中,维持稳定燃烧所需的最低氧气浓度(以氧气所占的体积百分数表示)叫氧指数.氧指数高表示材料不易燃,氧指数低表示材料容易燃烧.一般认为:氧指数<27%属易燃材料,27%≤氧指数<32%属可燃材料,氧指数≥32%属难燃材料.下面是一些常见物质氧指数.
| 可燃物 | 红磷 | 木炭 | 硫 | 蜡烛 | 铁丝 |
| 氧指数 | 0.5% | 4% | 4.5% | 5%~6% | 60% |
(1)写出铁丝在氧气中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)由上表可知铁丝是难燃材料(填“易燃”“可燃”或“难燃”)
(3)在测定空气中氧气含量的实验中,我们通常选择红磷燃烧而不选择木炭或硫的原因是木炭或硫燃烧后的产物为气体.
【反思与评价】
(4)如果一定要用木炭代替红磷做这个实验,只要对实验稍作改进即可,需要对实验改进的是将蒸馏水改成氢氧化钠溶液;
理由是:氢氧化钠溶液对二氧化碳的吸收效果比蒸馏水好.
(5)即使这样的改进,根据上表数据可知:仍然没有用红磷燃烧好,原因是:木炭氧气含量在4%以下就不能燃烧了,而红磷仅仅到0.5%以下才不能燃烧,使得氧气反应更充分.
18. 实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
【提出问题】双氧水分解快慢的影响因素有哪些?
【猜想与假设】猜想一:可能与二氧化锰的形状有关;猜想二:可能与温度有关.
【设计并实验】小王同学用8mL3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余);
(1)欲探究温度对”双氧水分解快慢“是否有影响,应该比较a(或b)和c(或d)(填“a”“b”“c”或“d”)的大小;若粉末状二氧化锰催化效果好,那么b(或d)>c(或a)(填“a”“b”“c”或“d”)
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积.
注意;若答对下列小题奖励4分,化学试卷总分不超过60分.
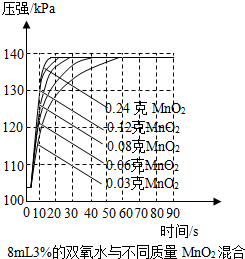
(3)小王同学还是用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响.他在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2.测得容器内压强的变化曲线如图所示(曲线的斜率表征催化反应的速率).请你观察图,并写出两条规律性结论:
①一定范围内,二氧化锰用量越多,双氧水分解越快;
②一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响.
 实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.【提出问题】双氧水分解快慢的影响因素有哪些?
【猜想与假设】猜想一:可能与二氧化锰的形状有关;猜想二:可能与温度有关.
【设计并实验】小王同学用8mL3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余);
| 实验编号 | 温度℃ | 二氧化锰的形状(均取0.4cm) | 收集到氧气的体积/mL(时间均为10s) |
| ① | 20 | 颗粒状 | a |
| ② | 30 | 粉末状 | b |
| ③ | 30 | 颗粒状 | c |
| ④ | 20 | 粉末状 | d |
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积.
注意;若答对下列小题奖励4分,化学试卷总分不超过60分.
(3)小王同学还是用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响.他在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2.测得容器内压强的变化曲线如图所示(曲线的斜率表征催化反应的速率).请你观察图,并写出两条规律性结论:
①一定范围内,二氧化锰用量越多,双氧水分解越快;
②一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响.