题目内容
2.现有八种物质,选择相应物质的字母序号填空:A.熟石灰 B.硬铝 C.一氧化碳 D.石油
E.生石灰 F.食盐 G.干冰 H.金刚石
(1)F可用作厨房调味品 (2)B可用作制造飞机
(3)G可用于人工降雨 (4)H可用来切割大理石
(5)D被誉为“工业的血液”(6)A可用于改良酸性土壤.
(7)C是煤气的主要成分 (8)E可用作食品干燥剂.
分析 物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可.
解答 解:(1)食盐可以用于调味品,故填:F;
(2)硬铝硬度大,氖腐蚀,可用作制造飞机,故填B;
(3)干冰升华吸热,能用于人工降雨,故填:G;
(4)金刚石硬度大,可用来切割大理石,故填H;
(5)石油是化石燃料,被誉为“工业的血液”,故填D;
(6)氢氧化钙(熟石灰)具有碱性,常用于改良酸性土壤,故填:A;
(7)一氧化碳是煤气的主要成分,故填C;
(8)生石灰能与水反应,可以用作干燥剂,故填:E;
答案:(1)F; (2)B; (3)G; (4)H;(5)D; (6)A;(7)C;(8)E.
点评 本题考查的是常见的物质的用途,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
12.门捷列夫说:“观察是第一步,没有观察就没有接踵而来的前进.”下列有关实验的现象描述正确的是( )
| A. | 一氧化碳通入澄清石灰水中,澄清石灰水变浑浊 | |
| B. | 打开浓盐酸的瓶塞时,瓶口冒白烟 | |
| C. | 在滴有酚酞的烧碱溶液中滴加稀盐酸,溶液由红色变成无色 | |
| D. | 在空气中点燃镁条,发出耀眼的强光,生成黑色固体 |
17.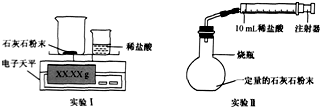 某校学习小组准备探究气体的测定和数据处理方法.
某校学习小组准备探究气体的测定和数据处理方法.
【提出问题】
如何利用石灰石(主要成分为CaC03)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定C02的质量和体积.
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaC03完全反应的实验现象是最后一次加稀盐酸后,无气泡冒出;
(2)实验Ⅱ中,先连接好装置并检查气密性,然后装好药品,最后将10mL稀盐酸快速推入烧瓶中.若稀盐酸是分几次缓慢推入的,则可能造成的后果是由于反应生成气体使装置中压强增大,再次推入较困难;
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯十石灰石粉末)+m(小烧杯十稀盐酸)],要计算生成C02的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯十反应后剩余物)
(4)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定):
根据以上实验过程和数据综合分析,最终生成C02的体积80 mL.
(5)该学习小组的同学采集了一块石灰石样品,将其敲碎后,称出6g放入烧杯内(烧杯质量为20g).然后加入50g稀盐酸(足量),充分反应后,再称量为73.8g(连烧杯一起).试回答:
①将石灰石样品敲碎的主要目的是增大反应物的接触面积,使反应更充分.
②该实验过程中,共产生CO2的质量2.2g.
③该石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留一位小数)
 某校学习小组准备探究气体的测定和数据处理方法.
某校学习小组准备探究气体的测定和数据处理方法.【提出问题】
如何利用石灰石(主要成分为CaC03)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定C02的质量和体积.
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaC03完全反应的实验现象是最后一次加稀盐酸后,无气泡冒出;
(2)实验Ⅱ中,先连接好装置并检查气密性,然后装好药品,最后将10mL稀盐酸快速推入烧瓶中.若稀盐酸是分几次缓慢推入的,则可能造成的后果是由于反应生成气体使装置中压强增大,再次推入较困难;
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯十石灰石粉末)+m(小烧杯十稀盐酸)],要计算生成C02的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯十反应后剩余物)
(4)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
(5)该学习小组的同学采集了一块石灰石样品,将其敲碎后,称出6g放入烧杯内(烧杯质量为20g).然后加入50g稀盐酸(足量),充分反应后,再称量为73.8g(连烧杯一起).试回答:
①将石灰石样品敲碎的主要目的是增大反应物的接触面积,使反应更充分.
②该实验过程中,共产生CO2的质量2.2g.
③该石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留一位小数)
7.用氢、氧、硫、铁四种元素中的若干种组成下列物质各二种,写出其化学式:
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | H2SO4、H2SO3 | Fe(OH)3、Fe(OH)2 | FeSO4、Fe2(SO4)3 | SO3、Fe2O3(合理即可) |
14.辰杰同学关于常见酸、碱、盐物质的说法不正确的是( )
| A. | 稀释浓硫酸时应先计算,再用量筒量取一定体积浓硫酸加入到装水的烧杯中,并用玻璃棒搅拌 | |
| B. | 将浓盐酸和浓硫酸敞口放置空气中溶液质量都会减少 | |
| C. | 烧碱、纯碱都可用于造纸、纺织工业 | |
| D. | 酸碱盐溶液能导电的原因是:酸碱盐在水溶液中形成了自由移动的离子 |