题目内容
12.工业上常使用氧炔焰,氧炔焰就是利用乙炔(C2H2)在氧气中燃烧放出大量热来焊接和切割金属.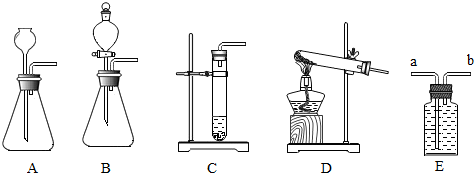
(1)实验室可用碳化钙(CaC2)固体和水反应来制取乙炔气体,同时生成氢氧化钙,写出制取乙炔的化学方程式;
(2)该反应必须严格控制加水的速度,以免剧烈反应放热引起发生装置炸裂,请从图中选择制取乙炔的最适合发生装置.
(3)已知乙炔是一种微溶于水的气体,如果用E装置来收集乙炔,则气体应该从b管口进入集气瓶内.
分析 (1)根据题意,碳化钙(CaC2)固体和水反应来制取乙炔气体,同时生成氢氧化钙,写出反应的化学方程式即可.
(2)根据题意,该反应必须严格控制加水的速度,以免剧烈反应放热引起发生装置炸裂,据此进行分析解答.
(3)乙炔是一种微溶于水的气体,如果用E装置来收集乙炔,即用排水法收集气体,进行分析解答,
解答 解:(1)碳化钙(CaC2)固体和水反应来制取乙炔气体,同时生成氢氧化钙,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(2)该反应必须严格控制加水的速度,以免剧烈反应放热引起发生装置炸裂,装置B可通过分液漏斗的活塞逐滴滴加液体,达到控制反应速率的目的.
(3)乙炔是一种微溶于水的气体,如果用E装置来收集乙炔,即用排水法收集气体,长导管是出水管,则气体应该从b管口进入集气瓶内.
故答案为:(1)CaC2+2H2O=Ca(OH)2+C2H2↑;(2)B;(3)b.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.实验室有一包固体混合物,含有Na2CO3、NaHCO3和NaOH三种物质,现取一定质量 的固体混合物,与100g溶质质量分数为7.3%的稀盐酸正好完全反应,则反应后所得溶液中( )
| A. | 氯化钠的溶质质量分数为11.7% | B. | 含有氯化钠的质量为11.7 g | ||
| C. | 溶液的pH小于7 | D. | 生成二氧化碳的质量为8.8 g |