题目内容
万州中学初三一班的学生为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验,请你与他们一起完成以下探究活动。(4分)
【对固体猜想】Ⅰ:全部是NaOH;Ⅱ:全部是Na2CO3;Ⅲ: 。
【查阅资料】经查阅资料可知,常见的盐溶液中,Na2CO3溶液显碱性,CaCl2溶液显中性
【实验和推断】
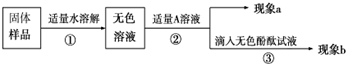
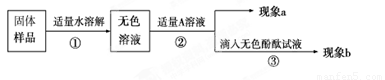
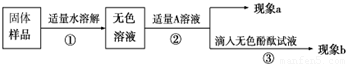
(1)向无色溶液中加入A溶液,现象a为有气泡产生,则A溶液是 ,说明氢氧化钠已经变质。
(2)由(1)可知氢氧化钠已经变质,重新取适量的无色溶液,加入足量的A(CaCl2溶液)除去Na2CO3,请写出这二者反应的化学方程式 , 当实验现象 (提示:现象a和b),则猜想Ⅲ成立。
【对固体猜想】 Na2CO3和NaOH
(1) HCl或者H2SO4 (合理即可)
(2) CaCl2 +Na2CO3 ===CaCO3 ↓ + 2 NaCl 现象a为白色沉淀,现象b为无色溶液变红
【解析】猜想Ⅲ:久置的氢氧化钠固体可能出现:不变质,固体仍为氢氧化钠;部分变质,固体为氢氧化钠和碳酸钠的混合物;全部变质,固体为碳酸钠;故答案为:NaOH和Na2CO3混合物;
(1)向溶液中滴加稀盐酸,盐酸与碳酸钠反应,生成氯化钠、水和二氧化碳,观察到有气泡产生,说明氢氧化钠已经变质;故答案为:HCl(或稀H2SO4等酸);
(2)向溶液中滴加氯化钙溶液,氯化钙与碳酸钠反应可生成碳酸钙沉淀和氯化钠,其化学方程式为:CaCl2 +Na2CO3 ===CaCO3 ↓ + 2 NaCl;如果固体为氢氧化钠和碳酸钠的混合物,滴入的氯化钙与面酸钠反应生成白色沉淀;滴入的酚酞遇氢氧化钠变成红色;故答案为:现象a有白色沉淀产生,现象b无色酚酞变红色。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案