题目内容
20. 物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?小明、小强按如图的装置进行探究:
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?小明、小强按如图的装置进行探究:(1)提出问题:化学反应前后,总质量是否发生改变?
(2)建立假设:化学变化前后总质量不变.
(2)查阅资料:
CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;
Ca2CO3+2HCl═CaCl2+H2O+CO2↑.
(4)设计实验:小明设计的实验装置和选用药品如A所示,小强设计的实验装置和选用药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
(5)得出结论:
①小明认为:在化学反应中,生成物的总质量与反应物的总质量相等;
小强认为:在化学反应中,生成物总质量与反应物总质量不相等.
②你认为小明的结论正确.
③导致另一个实验结论错误的原因是:小强的实验漏掉生成物的气体的质量.
小军认为,若将该装置进行改进也可以得出正确的结论,他改进的方法是将反应物放在密闭容器中进行.
分析 在表达质量守恒定律时,一定不要漏掉反应物或生成物的质量,特别是气体物质,容易忽略.选择另外两种药品验证质量守恒定律时,除了两种物质要反应外,最好不生成气体物质.
解答 解:②小明的结论是正确的,因为在质量守恒定律中,反应物的总质量等于生成物的总质量;
③小强的实验漏掉生成物的气体的质量;可将反应物放在密闭容器中进行实验.
答案:②小明;③小强的实验漏掉生成物的气体的质量,将反应物放在密闭容器中进行.
点评 在验证质量守恒定律时,很容易忽略气体的质量,不管是反应物还是生成物中气体的质量,有气体参加或生成的实验必须在密闭容器中进行,这点一定要注意到.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列图象能正确反映对应变化关系的是( )
| A. |  向一定量的二氧化锰中加入过氧化氢溶液生成气体的质量 | |
| B. |  加热氯酸钾和二氧化锰的混合物制取氧气,横坐标为加热时间 | |
| C. |  向一定量的大理石(杂质不参加反应)中加入足量的稀盐酸 | |
| D. |  向一定质量的稀盐酸中加入足量铁粉 |
8.化学反应前后,下列各项中肯定没有变化的是( )
①原子数目②原子的种类③分子的种类④原子质量⑤元素的种类⑥物质的种类⑦物质的总质量.
①原子数目②原子的种类③分子的种类④原子质量⑤元素的种类⑥物质的种类⑦物质的总质量.
| A. | ①②④⑤⑦ | B. | ①②⑤⑥ | C. | ①②③⑤ | D. | ③④⑤⑥⑦ |
12.地震发生后,饮用水源受到污染,为保证居民正常生活,用下述方法处理饮用水源:①消毒 ②自然沉降 ③过滤.处理的先后顺序是( )
| A. | ②①③ | B. | ②③① | C. | ③②① | D. | ③①② |
10.通过学习,我们知道有些物质混合后,虽然无明显现象产生,但确实发生了化学反应,如氢氧化钠溶液和二氧化碳,写出该反应的化学方程式CO2+2NaOH=Na2CO3+H2O.教材上是通过证明反应物二氧化碳的减少证明了反应的发生.某兴趣小组的同学认为还可以通过以下实验证明.请与他们一起完成实验方案的实施和评价.
①方案一:将二氧化碳通入盛有氢氧化钠溶液的试管中,再滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠溶液发生了反应.
②方案二:资料显示,常温下NaOH、Na2CO3分别在水和酒精中的溶解度
(单位:g/100g溶剂)如下所示:
将CO2通入饱和的NaOH乙醇溶液中,观察到有白色沉淀生成,证明二氧化碳与氢氧化钠溶液发生了反应.他们的推测依据是碳酸钠在酒精中的溶解度<0.01g.
③上述两个方案在设计思想上的相同点是依据碳酸钠具有的不同性质设计实验.
①方案一:将二氧化碳通入盛有氢氧化钠溶液的试管中,再滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠溶液发生了反应.
②方案二:资料显示,常温下NaOH、Na2CO3分别在水和酒精中的溶解度
(单位:g/100g溶剂)如下所示:
| 溶剂 | NaOH | Na2CO3 |
| 水 | 109 | 21.8 |
| 酒精 | 17.3 | <0.01 |
③上述两个方案在设计思想上的相同点是依据碳酸钠具有的不同性质设计实验.
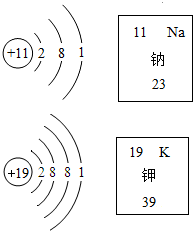 如图分别是钠和钾两种原子的结构示意图和它们在元素周期表中的部分信息.
如图分别是钠和钾两种原子的结构示意图和它们在元素周期表中的部分信息.