题目内容
5. 某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:①取一段镁带样品,准确称得其质量为0.030g.
②往量气管内装水至低于刻度“0”的位置.按图所示(未装药品)装配好仪器.
③检查装置气密性.
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞.
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置.
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应.
⑦待冷却至室温后,再次记录量气管中液面位置.
⑧算出量气管中增加的气体体积为23.96mL.
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和.
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式Mg+H2SO4═MgSO4+H2↑.
(2)能否用托盘天平称量0.030g镁带样品,不能(填“能”或“不能”).
(3)若不改变温度,如何用较简单的方法检查如图所示装置的气密性?把玻璃管下移一段距离,使玻璃管和量气管中的水形成一定的液面差,如果一段时间后液面差保持不变,则说明装置不漏气;反之,则表示装置漏气.
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果否(填“是”或“否”).理由是因为试管中留有的氢气体积等于从试管中排出的空气体积,所以对实验最终结果没有影响.
(5)经换算,该实验获得的氢气质量为0.0020g.该镁带中单质镁的质量分数是80%.(要求:写出完整的计算过程)
分析 (1)镁与硫酸发生置换反应,反应生成硫酸镁同时放出氢气;
(2)称量0.030g镁需要精确度为0.001g的天平,而托盘天平的精确度一般为0.1g,不能称量0.030g镁带样品;
(3)在不改变温度的情况下,可通过抬高或降低玻璃管内液面而产生压强差而检查该装置的气密性;
(4)根据“同温同压下,不同气体混合后体积等于混合前各气体体积之和”可知,装置内气体体积为空气的体积与生成氢气体积之和,试管内的留有的氢气与排出的空气体积相等,并不影响测定结果;
(5)根据反应的化学方程式,由产生氢气质量计算镁带中镁的质量,进而计算该镁带中单质镁的质量分数.
解答 解:(1)镁与硫酸发生置换反应生成硫酸镁和氢气,反应的化学方程式为Mg+H2SO4═MgSO4+H2↑;
故答案为:Mg+H2SO4═MgSO4+H2↑;
(2)托盘天平只能精确到0.1g,因此不能使用托盘天平称量出0.030g镁;故答案为:不能;
(3)抬高玻璃管会使装置内气体压强增大而降低玻璃管则会使气体压强减小,通过压强的改变并能维持这种改变,可检查装置的气密性;
故答案为:把玻璃管下移一段距离,使玻璃管和量气管中的水形成一定的液面差,如果一段时间后液面差保持不变,则说明装置不漏气;反之,则表示装置漏气;
(4)根据“同温同压下,不同气体混合后体积等于混合前各气体体积之和”,留在试管内的氢气排出等体积的空气而使装置内气体体积总和不变,因此,此部分氢气并不影响对产生氢气的体积的测量;
故答案为:否;因为试管中留有的氢气体积等于从试管中排出的空气体积,所以对实验最终结果没有影响;
(5)设镁的质量为x
Mg+H2SO4═MgSO4+H2↑
24 2
x 0.0020g
$\frac{24}{2}=\frac{x}{0.0020g}$
x=0.024g
该镁带中单质镁的质量分数=$\frac{0.024g}{0.030g}$×100%=80%
故答案为:80%.
点评 本题以创新实验装置的形式,对仪器的使用、装置气密性的检查、化学计算、实验方案评价等进行考查,需要一定的思考灵活.

 智慧小复习系列答案
智慧小复习系列答案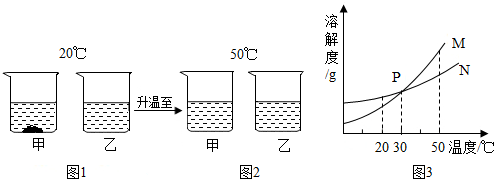
| A. | 图1中甲溶液溶质质量分数比乙溶液大 | |
| B. | 图2中甲、乙溶液一定都是饱和溶液 | |
| C. | 图3中表示甲的溶解度曲线是M | |
| D. | 30℃时,甲、乙溶液溶质质量分数不相等 |
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
(2)若实验②比实验①的“待测数据”更小(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若衡量得到0.5g黑色粉末,再将黑色粉末放入试管中,向试管中倒入适量的双氧水,观察到大量气泡.(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
某化学兴趣小组的同学开展了以下探究活动.

【实验探究一】将呼出气体通过下图A 中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如下图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较木条燃烧的剧烈程度 来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是吸收呼吸产生的二氧化碳,同时生成氧气
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH;
猜想Ⅱ:溶质是Na2CO3
猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,产生Na2CO3 的现象,证明猜想Ⅰ不成立.
浑浊同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
| 实验步骤和现象 | 结论 |
| 取无色溶液少许于试管中,向其中加入过量的氯化钙溶液,有白色沉淀产生,过滤,再向滤液中加入无色酚酞试液,溶液变红 | 猜想Ⅲ成立 |
| A. | 铁片、铜片 | B. | 铜片、铝片 | C. | 镍片、锌片 | D. | 铁片、镍片 |




